Etiquetas
#pandemia #COVID-19 #triaje #toma de decisiones #comorbilidades #cuidados paliativos #Dolor crónico #Neurocirugía #Síndrome de Fracaso de Cirugía Espinal Lumbar #anestesia espinal unilateral #dosis mínima #lateralización #cirugía traumatológica ambulatoria #nervio pudendo #neuralgia #radiofrecuencia pulsada; ultrasonido. #dolor #dolor neuropatico #topiramato #dolor agudo postquirúrgico #dolor incisiona #anestesia #niños #dolor agudo #dolor quirurgico #modelos y teorias #enfermeria #noticias #Investigación en Servicios de Salud #Rehabilitación #ansiedad #emociones #miedo #tristeza #Parche #Buprenorfina #Fentanilo #problemas sociales #síndrome pediátrico inflamatorio multisistémico #fibromialgia #narrativas #experiencia #Afrontamiento #estados emocionales #dolor de espalda #Cuidado paliativo #opioidesRevista El Dolor 44 | Noviembre 200 - Año 14 | Colaboraciones Especiales
Consecuencias Clínicas de la Estimulación Sensorial Persistente: La Sensibilización Espinal Segmentaria
Dr. Pedro Romero V.³
Médico Anestesiólogo Lima - Perú peterpain@terra.com.pe
Introducción
Introducción
Existían algunas creencias erradas respecto al dolor, las cuales se han ido modificando a la luz de los conocimientos actuales. Por ejemplo, se decía que "el estado doloroso refleja la respuesta a la activación de un sistema específico, anatómicamente definido", también que "la magnitud y calidad de la respuesta dolorosa guarda proporción con la magnitud del estímulo". Actualmente sabemos, por la experiencia clínica, que esto no siempre es verdad. El sistema de respuesta al estímulo nociceptivo dista de estar
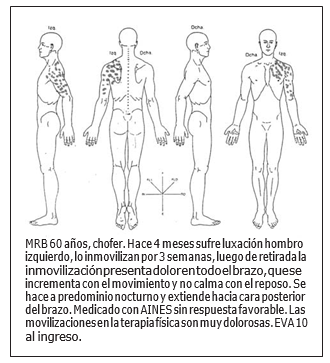
exactamente definido y, fundamentalmente, existe una disociación frecuente entre la magnitud del estímulo físico y la intensidad, características y duración de la respuesta dolorosa1. Así, estímulos nociceptivos persistentes pueden inducir cambios en los procesos periféricos y centrales, principalmente en médula espinal, que conducen a esta última, a un estado de sensibilización anormal, que se traducirá clínicamente en dolor espontáneo, hiperalgesia y alodínea.
Con el fin de graficar las consecuencias de estos procesos, revisemos sumariamente algunos casos clínicos:
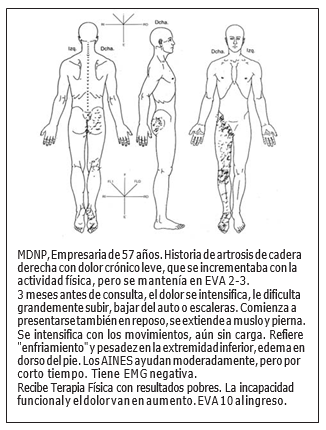

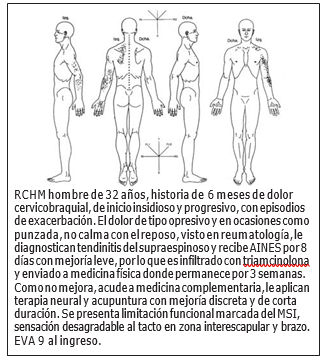

¿§ué Tienen en Común Estos Casos?
Observamos características comunes, tanto en lo descrito por los pacientes como en lo encontrado al examen: (a) el síntoma cardinal es el dolor, espontáneo o evocado; (b) es regional, ya que este dolor sobrepasa la localización esperada en función de la causa originaria, pudiendo tomar un patrón cervicocraneal, cervicobraquial o lumbociático; (c) es un síndrome, ya que permite englobar en ella una serie de síntomas y signos clínicos que pueden no tener una etiología común; y (d) es complejo debido a las diversas formas de presentación del cuadro. Adicionalmente, si tratamos de definir ante qué tipo de dolor estamos, concluimos que es de naturaleza neuropática, que en contraste con el dolor nociceptivo, es descrito como "quemante", "como descargas", de presentación espontánea, profundo, continuo, con exacerbaciones paroxísticas, sin causa aparente, o en respuesta a movilización o la presión de la extremidad afectada u otros estímulos, y que no guarda la proporción esperada en relación con la causa subyacente aparente, también debido a que al examen clínico encontramos alodínea e hiperalgesia.
Etiología
La SES reconoce por lo general un antecedente de origen traumático, como lesiones del hombro, esguinces de tobillo, lesiones por aplastamiento, fracturas e inmovilizaciones

prolongadas. En ocasiones, puede complicar problemas dolorosos somáticos crónicos como la artrosis de cadera o rodilla, otros casos tienen antecedentes de procedimientos quirúrgicos, de mayor o menor complejidad; lo hemos visto después de cirugía por síndrome del túnel del carpo, reparación de tendones en mano. También acompaña a condiciones tales como hernias del núcleo pulposo, estenosis vertebrales, disfunciones intervertebrales mínimas, puntos gatillo miofasciales, después de accidente cerebro vascular, después de cirugía de by-pass coronario y algunos problemas viscerales, en el cáncer de pulmón. También es cierto que en ocasiones aparece sin un antecedente previo y no podemos determinar la causa.
Fisiopatología
Se han propuesto varias hipótesis intentando explicar el mecanismo de producción de la Sensibilización Espinal Segmentaria. Sostenemos que su punto de partida es la estimulación sensorial periférica persistente que, asociada a la falla de los mecanismos inhibitorios, conduce a la hiperexcitabilidad de ciertas neuronas del asta posterior de médula espinal. Esto constituye la base de la "sensibilización central", cuya traducción clínica es la SES.
A continuación, un breve recordatorio para entender estos conceptos de sensibilización.
Sensibilización Periférica
La lesión tisular activa por un lado la cascada del ácido araquidónico, siendo sus productos finales las prostaglandinas y los leucotrienos; por el otro lado, provoca la conversión enzimática del quininógeno en bradicinina por acción de las
calicreinas. Adicionalmente, las citoquinas, principalmente la interleuquina-1þ (IL-1þ), IL-8 y el Factor de Crecimiento Tumoral a (TNF-a) inducen la formación de receptores B1 de bradicinina, favoreciendo así su producción y liberación. La bradicinina activa directamente a los nociceptores y las prostaglandinas, principalmente las PGE² y PGI², sensibilizan a los nociceptores a la acción de la bradicinina. Estos mediadores químicos, asociados a otros, conducen a un incremento en la actividad de los nociceptores conocida como "hiperalgesia primaria" (debido a que ocurre en el sitio del daño tisular), responsable de que los nociciceptores exhiban actividad espontánea, disminución de su umbral de excitación e incremento en la respuesta al estimulo supraumbral.
Sensibilización Central
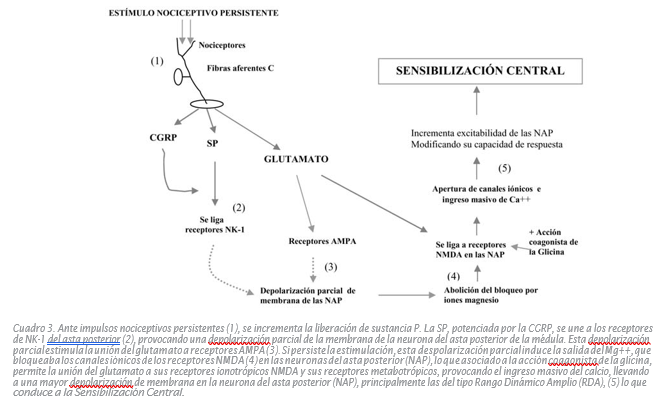
El estímulo en los nociceptores provoca liberación de Sustancia P (SP) y glutamato desde sus terminales pre-sinápticas, las que se ligan a sus receptores post-sinápticos en las neuronas de segundo orden del asta posterior, principalmente en las de Rango Dinámico Amplio (RDA).
La despolarización parcial de la membrana, provocada por la unión de la SP a su receptor de neuroquinina-1 (NK-1), acción que es facilitada por la CGRP, permite que el glutamato actúe primero sobre los receptores No-NMDA como los alfa-amino- 3-hidroxi-5-metil-4-isoxazolpropionato (AMPA) y kainato (KAI). Los receptores N-metil-diaspartato (NMDA) generalmente se mantienen casi inactivos en la transmisión sináptica "normal", debido a que sus canales están parcialmente bloqueados por Magnesio. Si la estimulación sensorial persiste, se libera este bloqueo y el glutamato se une con los receptores NMDA, lo que

a su vez permite el ingreso masivo del ion calcio. El ingreso del Ca++ lleva a la despolarización continua de las neuronas nociceptivas del asta posterior (Mayer and Miller 1990), provocando la suma temporal lenta de respuestas de estas neuronas de segundo orden, fenómeno conocido como "wind- up" que las lleva a la sensibilización central progresiva, lo que incrementa su frecuencia de descarga espontánea, expande sus campos receptivos, disminuye su umbral de respuesta, permitiendo ahora que puedan ser activadas por potenciales excitatorios post-sinápticos que eran inefectivos (sub-umbrales) previamente; se origina además una respuesta exagerada a los estímulos somatosensoriales mecánicos y térmicos subsiguientes. Estos eventos descritos, son la base para el dolor espontáneo, la hiperalgesia y la alodinea.
Expresión de Genes en el Asta Posterior de Medula Espinal El ingreso masivo del calcio al intracelular de la segunda neurona, mediante los mecanismos ya descritos, potencia la actividad de dos enzimas: la óxido nítrico-sintetasa (NOS) y la fosfolipasa C (PLC). El óxido nítrico (ON) sintetizado por acción de la NOS se mueve extracelularmente e incrementa la liberación de neurotransmisores desde las terminales presinápticas. La activación de la PLC promueve la formación de los segundos mensajeros inositol trifosfato (ITP3) y diacilglicerol (DAG). El ITP3, además de liberar calcio desde depósitos internos, lleva a la formación de ácido araquidónico y sus metabolitos, los
cuales por acción de la ciclo-oxigenasa (COX) se convierten en prostaglandinas generadas centralmente. Esto último sostiene la idea de la acción central de los AINES. El DAG estimula la translocación de la proteincinasa C (PKC) desde el citoplasma hacia la membrana celular. La PKC activada, incrementa la excitabilidad de la membrana, principalmente de los receptores NMDA, e induce también la formación de genes tempranos inmediatos (IEG) como el c-fos y c-jun.
Las proteínas, productos de estos IEG, pueden actuar como tercer mensajero (transcripción) y controlar la expresión de otros genes comprometidos en la síntesis de factores de crecimiento, proteínas de canales, péptidos y enzimas. La expresión de los IEG está relacionada con la actividad neuronal, y el número de neuronas fos-positivas se correlaciona con el grado de dolor.
Memoria del Dolor
Muchos de los mecanismos neurales movilizados por el estímulo doloroso en el SNC de los vertebrados son muy primitivos; se encuentran presentes también en las neuronas de formas animales muy simples. Estos mecanismos, como la activación de canales iónicos, segundos mensajeros o expresión de genes, también son los mediadores de la reacción exagerada del molusco aplisia a un choque eléctrico reiterado. Así, Sun y Carr3 afirman que, como los vertebrados y los moluscos tienen antecesores comunes, el incremento de la respuesta a estímulos
nociceptivos sucesivos ha constituido una verdad biológica conservada durante millones de años. Podemos asumir entonces, que la tendencia de los estímulos nociceptivos prolongados a transformar el sistema nervioso desde un estado basal a un estado de sensibilización es una forma de inestabilidad programada dentro del sistema nervioso.
A diferencia de los organismos primitivos, el ser humano tiene mecanismos inhibitorios que le permiten modular la respuesta dolorosa.
Mecanismos para Control del Dolor
Mecanismos segmentarios: Las interneuronas encefalinérgicas de la sustancia gelatinosa, que reciben sinápsis desde las fibras gruesas (como las Aþ), regulan el ingreso desde las fibras delgadas hacia las neuronas de la lámina V, sirviendo como mecanismo de compuerta. Es la base de la analgesia conseguida con estímulos de baja intensidad, como al aplicar TENS o vibración sobre la piel. Por esta razón ayuda sacudir la mano cuando uno se la quema, debido a que esto activa principalmente fibras gruesas. El control del dolor en este caso está organizado segmentariamente.
El ácido y-Aminobutírico (GABA) y glicina se liberan en el asta posterior como un mecanismo compensatorio para limitar la nocicepción en respuesta a impulsos aferentes nociceptivos. El GABA se origina principalmente en las interneuronas GABAérgicas. Las fibras aferentes delgadas (como las C) que contienen CGRP, hacen sinapsis con las dendritas de las
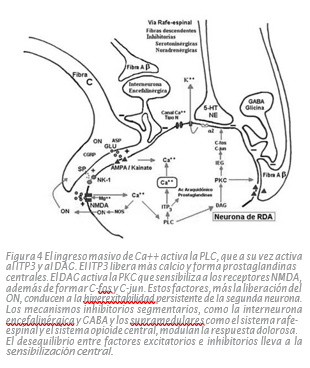
interneuronas GABAérgicas del asta posterior (Hayes y Carlton 1992). Otra fuente del GABA que se libera en el asta posterior son las proyecciones medulares de neuronas GABAérgicas en la zona ventromedial del bulbo raquídeo (Antal 1996). Esta vía bulboespinal se activa en condiciones de nocicepción persistente. Las interneuronas conteniendo GABA hacen sinapsis con las fibras Aþ y la reducción o pérdida de la actividad de estas interneuronas produce la alodínea.
Mecanismos supramedulares: La estimulación eléctrica de la sustancia gris periacueductal (PAG) del mesencéfalo produce analgesia. Este control descendente es mediado por una vía de la PAG hacia neuronas que contienen serotonina (5-HT) en el núcleo magno del rafe (NRM), localizado en el bulbo raquídeo. Estos axones con 5-HT (vía rafe-medular), que vienen del núcleo magno del rafe, inhiben la descarga de las neuronas de las láminas I y II del asta posterior.
Existe también un control inhibitorio descendente paralelo que es noradrenérgico. Este último circuito puede ser el lugar de acción de los antidepresivos tricíclicos en el tratamiento del dolor neuropático.
Sustancias opioides: Los receptores opioides se concentran en la PAG y el asta posterior. Los receptores opioides pre-sinápticos, cuando son activados por sus agonistas, hiperpolarizan (inhiben) las terminales de las fibras C, al abrir los canales de potasio. Esta reducción en la excitabilidad significa que la liberación de neurotransmisores como la Sustancia P, glutamato y CGRP se reducen y como consecuencia, el mensaje doloroso se reduce en el primer relevo (Dickenson 1994). Cerca del 75% de los receptores opioides espinales se encuentran en estos lugares pre sinápticos. Tres familias de opioides endógenos han sido descritas: encefalinas, dinorfinas y þ-endorfinas. Las endorfinas se liberan por dolor y por estimulación eléctrica cerebral. El efecto placebo, en cuanto a analgesia, y la acción de la acupuntura, se relacionan con la activación de este sistema endógeno de control del dolor. Los antagonistas opioides (naloxano) revierten el efecto analgésico, tanto del placebo, como de la acupuntura y la estimulación eléctrica cerebral. Las þ-endorfinas, que se originan en el eje hipotálamo-hipófisis, se fijan a los receptores opioides en la PAG. Este proceso activa el control inhibitorio descendente que se inicia en la PAG y termina en el asta posterior de médula. El estado de hiperalgesia espinal inhibe la acción de los opioides.
Clínica
El síntoma dolor, definido como agudo, penetrante, como "tirones", a veces quemante, regional, usualmente espontáneo, que puede desencadenarse o exacerbarse a la presión, a la movilización articular activa o pasiva, con el estrés o las variaciones de temperatura. Es el síntoma inicial del síndrome, sigue inicialmente un patrón dermatomal y es aparentemente desproporcionado al factor desencadenante. Este dolor puede provocar dificultad en la marcha, porque se incrementa al apoyar el miembro inferior comprometido; o afectar la función del hombro o la mano, cuando el compromiso es del miembro superior. El origen del dolor no se puede definir con claridad, pero sí los niveles medulares comprometidos.
La intensidad del dolor es evaluada mediante la Escala Visual Análoga (EVA) y su distribución mediante el punteado sobre la silueta.
Ahora tenemos que evaluar y cuantificar mediante el examen clínico los signos que conforman este síndrome espinal segmentario. Salta a la vista que los métodos de exploración de la neurología clásica, como son: evaluación de los reflejos, la sensibilidad, la fuerza muscular, el tono y el trofismo no nos bastan. Estas pruebas están encaminadas a buscar daño, entonces debemos recurrir a una semiología nueva, dirigida a evaluar irritación o hiperexcitabilidad.
El año 1961, el Dr. Robert Maigne, en Francia, bajo el título de "síndrome vertebral segmentario célulo-tenoperióstico-miálgico" describió un grupo de modificaciones palpables en la textura y sensibilidad de los tejidos blandos: la palpación sistemática de los planos cutáneos mediante el "pinzado-rodado" muestra la sensibilidad del dermatoma o parte de él (celulálgia); el examen de los músculos muestra "cordones miálgicos" o puntos gatillo, dolorosos a la presión, localizados siempre en los mismos músculos pertenecientes al miotoma comprometido, incluso en la misma porción del músculo; la palpación también provoca dolor en las inserciones tendinosas y el periostio correspondientes al esclerotoma. Estas manifestaciones, al parecer consecuencia del bombardeo nociceptivo constante que lleva a las neuronas localizadas en el mismo segmento medular a un estado de facilitación, el cual se manifiesta con las respuestas motoras, autonómicas y sensoriales descritas. El origen de dicho bombardeo nociceptivo sería el segmento vertebral que presenta el "desarreglo intervertebral menor" (DIM).
El Dr. Chan Gunn (1979) en Canadá, sostiene también que el llamado "síndrome de dolor miofascial" no es de origen somático sino neuropático, específicamente por radiculopatía, y que mediante el examen apropiado encontraremos las manifestaciones sensoriales (hiperpatía y alodinea), motoras (acortamiento muscular, limitación del rango de movimiento, entesopatía) y autonómicas (vasoconstricción, reflejo pilomotor, actividad sudomotora, cambios tróficos y el trofoedema) asociadas. Afirma que la Espondilosis es la primera causa de esta radiculopatía, sostiene que el primer signo es el acortamiento muscular, que precede al dolor. Este acortamiento, mal llamado "espasmo", estresa mecánicamente las inserciones musculares causando "tendonitis" o "epicondilitis", que el acortamiento en músculos que actúan a través de una articulación incrementan la presión articular pudiendo provocar artralgias, el acortamiento de músculos paraespinales condiciona "síndromes facetarios", estenosa los agujeros intervertebrales irritando la raíz nerviosa y cerrando el círculo vicioso. Gunn describe las manifestaciones autonómicas de la radiculopatía, especialmente el tono incrementado en los músculos lisos de los vasos linfáticos que llevan al edema subcutáneo local (edema "neurogénico" o trofoedema) confirmado por el efecto de peau d' orange y la identación persistente al presionar con un elemento romo como la cabeza de un fósforo.
En 1998, el Dr. Andrew Fischer, de EEUU, describe la teoría del "PENTAD" dándole una explicación mecánica, compresiva radicular a los síndromes dolorosos regionales. Fischer, además de describir las manifestaciones motoras, sensitivas y simpáticas segmentarias, propone la cuantificación del umbral doloroso a la presión mediante su algómetro y su más grande aporte es la técnica de inyección que denomina "bloqueo paraespinoso" que constituye la piedra angular del tratamiento del Síndrome Espinal Segmentario (SES).
Con los datos previos, podemos sistematizar el examen de la manera siguiente:
Dermatoma
Tejido: Piel.
Prueba: Rascado con clip.
Técnica: La punta de un clip abierto es arrastrado lentamente a través de los bordes del dermatoma. Se le pide al paciente que indique si la sensación cambia a desagradable o agudo. Se debe mantener un ángulo de 45° y una presión constante de 40 gramos.
Respuesta: Hiperalgesia cutánea sobre dermatoma comprometido.
Tejido: Celular subcutáneo.
Prueba: Pinzado-rodado.
Técnica: Se coge entre el pulgar y la punta de los dedos un pliegue de piel y se hace rodar desplazando el tejido entre los dedos. Se debe realizar bilateral
Esclerotoma
por lo general el mismo punto del lado opuesto. El UDP es la mínima cantidad de presión que provoca dolor. Si utilizamos algómetro, se considera anormal si es inferior a 2 kg/cm² en relación al punto control. El presionar el punto más sensible, a menudo reproduce el dolor percibido por el paciente y su patrón referido, también puede desencadenar la respuesta de contracción brusca local (twitch), descrita con precisión por la Dra. Janett Travell. Otras evaluaciones podrían ser los reflejos osteotendinosos, que en ocasiones los encontramos incrementados; la fuerza muscular, usualmente normal, podría encontrarse disminuida por fenómenos inhibitorios reflejos o por dolor. Los reflejos los evaluamos con el martillo y la fuerza mediante el dinamómetro o usando pruebas musculares manuales.
y simétricamente: de arriba hacia abajo en el tronco y transversalmente en las extremidades.
Respuesta: La maniobra es muy dolorosa (celulálgia), el pliegue de la piel está engrosado, presenta "piel de naranja" y su deslizamiento es dificultoso.
Miotoma
Prueba: Acortamiento muscular.
Técnica: Desplazando lenta y gentilmente el músculo comprometido en su rango de movimiento hasta encontrar resistencia.
Respuesta: Está limitado el rango de movimiento y/o se acompaña de dolor. Se puede utilizar goniómetro para cuantificar el rango y la EVA para la intensidad del dolor.
Prueba: Bandas tensas.
Técnica: En músculos planos, como el infraespinoso, palpamos con los dedos ligeramente flexionados, frotando las fibras musculares relajadas, perpendicular a su orientación. En músculos voluminosos, como el bíceps o trapecio, realizamos palpación en pinza.
Respuesta: Se aprecian cordones indurados, generalmente dolorosos a la palpación, conformada por grupos de fibras musculares contraídas, usualmente en toda la longitud del músculo. Se encuentran en músculos pertenecientes al mismo miotoma cuando se ha establecido la SES.
Prueba: Umbral doloroso a la presión.
Técnica: Evaluado mediante la presión con el extremo distal del dedo pulgar, aplicando una presión de
± 4 kg. (que blanquea el lecho ungueal). Utilizamos el algómetro de Fischer, más aún si queremos cuantificar con más exactitud.
Respuesta: Umbral doloroso a la presión (UDP) disminuido comparado con un punto control normosensible,
Se refiere al dolor provocado a la palpación de estructuras como tendones, periostio de prominencias óseas o estructuras cápsuloligamentosas.
Generalmente se evidencia al examen, pero a veces como dolor espontáneo. Puede originarse como consecuencia de la sensibilización de su inervación y desaparecer con el tratamiento de la SES, o corresponder a fenómeno local, por sobrecarga de los músculos comprometidos, en cuyo caso responde al tratamiento local.
Maigne presenta una serie de "tendinitis" o "bursitis", que en realidad corresponden muchas veces a fenómenos de sensibilización medular.
Porción larga del bíceps C5-C6 Pubalgia D12-L1
Epitróclea C8
Trocánter L5
Angulo superior de escápula C4 Pata de ganso L4
Maigne considera el dolor a la presión sobre la apófisis espinosa, sobre el ligamento interespinoso y la fricción paraespinosa dolorosa como manifestaciones de la disfunción vertebral local. Fischer, afirma que el dolor al presionar el ligamento interespinoso es consecuencia del "desgarro" y es el punto de partida de su PENTAD, sosteniendo un origen mecánico de la SES. Para nosotros, son manifestaci ones de la sensibilización de la rama posterior del nervio raquídeo, y por lo tanto, lo incluimos en el examen como parte de la SES.
La limitación dolorosa de la movilidad articular puede reflejar la alodinea de las estructuras cápsuloligamentosas.
Sistema Autónomo: Disfunción Simpática
Prueba: Microtrofoedema.
Técnica: Se realiza presión sostenida por unos segundos con la cabeza de un fósforo o el capuchón de una aguja hipodérmica sobre la zona del dermatoma comprometido, preferiblemente
dermatoma comprometido, preferiblemente también sobre el lado indemne para comparación.
Respuesta: La depresión o fovea permanece varios minutos luego de suspender la presión. En casos puede observarse a simple vista la piel distendida y el borramiento de los pliegues cutáneos y las prominencias tendinosas. Fischer preconiza realizar la presión con la punta del algómetro usando una fuerza de 3 kg mantenida por 3 segundos.
Prueba: Conductancia eléctrica de la piel (CEP) Técnica: Se hace deslizar lentamente la punta del equipo a través de los dermatomas a evaluar.
Transversalmente en las extremidades y longitudinalmente en la zona axial paraespinosa.
Resultado: La CEP está incrementada sobre las zonas hiperalgésicas, tales como el dermatoma comprometido con la Sensibilización Espinal Segmentaria. Refleja cambios simpáticos sobre la microcirculación y las glándulas sudoríparas. Su ventaja es que su medición es independiente de la reacción del paciente, a diferencia de la evaluación de la sensibilidad mediante el rasguño con la punta del clip, además se puede cuantificar midiendo el cambio de la conductancia en microamperios.
Otras manifestaciones de hiperactividad simpática lo constituyen las alteraciones vasomotoras, como la aparición de cianosis distal o el dermografismo; la alteración de la temperatura cutánea, que la describen mayormente como de frialdad y, en algunos casos, como aumento de temperatura. Ocasionalmente se presentan alteraciones sudomotoras, habitualmente aumento de sudoración, que puede ser parcelar y se exacerba con el estrés (como instantes antes de realizarle un bloqueo paraespinoso). Hemos observado también pérdida del vello sobre el dermatoma comprometido, comprobando lo descrito por Gunn.
Consideraciones complementarias sobre la evaluación de la SES
- El signo que se presenta con más frecuencia y es más sensible para detectar SES es la celulálgia evaluada mediante el pinzado-rodado de la piel.
- La piel, el periostio y músculos del tronco inervados por el ramo primario posterior son más sensibles, reaccionan tempranamente y con más frecuencia a la irritación radicular.
- El espasmo muscular, las bandas tensas y los puntos dolorosos a la presión se presentan con distribución miotomal.
- Los músculos que comparten inervación múltiple presentan las bandas tensas y los puntos gatillo en la porción del músculo que corresponde a la raíz comprometida.
- Muchas veces, la zona reactiva en piel corresponde sólo con parte del dermatoma.
Tratamiento
Bloqueo paraespinoso (BPE): Realizado en el nivel del segmento espinal sensibilizado. En la técnica preconizada por Fischer (1998) se esparce lidocaína 1% a lo largo de la apófisis espinosa, en el espacio entre ésta y el músculo paraespinal adyacente, seguido luego por la inyección de los ligamentos supra/interespinosos "desgarrados", los cuales él considera como el foco irritativo que con frecuencia inician el PENTAD, que a su turno provoca la compresión radicular cuya consecuencia es la sensibilización segmental (radicular)6. Nosotros, al considerar que el origen de la SES no siempre es mecánico sino disfuncional neurológico, teorizamos que el BPE lo que consigue es un bloqueo de conducción de la rama posterior, que a su vez "desensibiliza" el segmento y, por lo tanto, "apaga" las manifestaciones de la SES en el miotoma, esclerotoma, dermatoma y sistema simpático. Por este motivo, no inyectamos el ligamento interespinoso, salvo que siga sensible luego del BPE. Usamos lidocaína a 2% sin preservantes, 1.5 cc a nivel cervical y 4 cc a nivel lumbar, diluido en 2 cc en el primer caso, y 5 cc en el segundo, de cloruro de sodio al 0.9%, que se coloca introduciendo una aguja calibre 25 paralela y adyacente a la apófisis espinosa del nivel comprometido, lo más cercana a la lámina subyacente. Se inyecta el 50% de la solución, el otro 50% se esparce en partes iguales hacia arriba y hacia abajo del nivel principal. Creemos que el volumen suple a la precisión de la inyección.
Como ha sido comunicado por muchos que emplean la técnica de Fischer, como Imamura, Cassius, Nakazato, y recientemente por Romero, Becerra y Celis8, la remisión de las manifestaciones de la SES es usualmente inmediata.
Inactivación de Puntos Gatillo
Luego del BPE examinamos nuevamente las bandas tensas dolorosas en los músculos del miotoma comprometido, igualmente las inserciones tendinosas, ligamentos, bursas, etc., del esclerotoma y la piel del dermatoma. La mayoría de veces estas manifestaciones han desaparecido; en los casos que permanezcan los Puntos Gatillo, ya sea por ser el origen periférico del bombardeo sensorial persistente o por haberse "estructurado", es decir, que el fenómeno de disfunción neurológica, al prolongarse en el tiempo, ha condicionado fenómenos de perpetuación local como la "crisis de energía". En estos casos, "desgatillamos" los puntos musculares y/o tendinosos, mediante la técnica de agujamiento e inyección con lidocaína o mediante la técnica de "aguja seca", usando agujas de acupuntura, también podemos infiltrar el subcutáneo en las zonas de celulalgia persistente. El procedimiento es seguido de estiramientos, preferiblemente por inhibición recíproca, luego aplicamos compresas calientes. En los casos que exista sangrado durante el procedimiento, preferimos las compresas frías.
En algunos casos tempranos, donde la SES es originada en Puntos Gatillo miofasciales o entesopatías, si el problema se trata primero y en forma efectiva, todo el síndrome de sensibilización tiende a resolverse. Esto es particularmente cierto en casos de cervicobraquialgia originado en el hombro.
Rehabilitación
La terapia física asociada con la terapia ocupacional juegan un rol importante en la restauración funcional. La meta es incrementar en forma gradual la fuerza y flexibilidad,
empezando con movimientos amplios suaves. Aunque el paciente esté reticente de participar ya que le provoca dolor, le haremos notar que a medida que mueve, el dolor va disminuyendo. Reforzar la idea que el soporte del peso activo y progresivo, o la movilización activa y uso funcional de la extremidad superior, llevarán a una normalización gradual de las respuestas a los estímulos sensoriales, disminuyendo, por ejemplo, la alodínea mecánica (dolor al movimiento articular) y normalizando progresivamente los procesos alterados en el SNC. En TO se pueden aplicar técnicas de compresión y distracción que estimulan la extremidad afectada sin producir movimiento articular. Se puede friccionar la parte afectada con un cepillo, aumentando poco a poco la presión, friccionando en círculos. También se utiliza percusiones, vibración. Luego se aumenta el peso soportado por las articulaciones.
La estimulación nerviosa eléctrica transcutánea (TENS): Puede aliviar el dolor si la SES está limitada a la distribución de una raíz o un nervio periférico.
Fármacos
Gabapentina (neurontin)-Propiedades anticonvulsivantes y efecto antineurálgico; su mecanismo de acción no se conoce con exactitud. Estructuralmente está relacionado con los receptores GABA, pero, no interactúa con ellos.
Dosis: desde 300 mg PO hs hasta 300 a 600 mg PO tid. Interacción: los antiácidos reducen su biodisponibilidad, por lo que se aconseja administrar por lo menos 2 h luego de tomar antiácidos.
Precaución: No interrumpir bruscamente su administración, hacerlo progresivamente; usar con precaución en insuficiencia renal. No utilizar en gestantes.
Amitriptilina (tryptanol) - ha demostrado efectividad en dolor neuropático.
Dosis: Usamos de 12.5 a 50 mg PO hs, por lo general no usamos más de 25 mg, aunque otros autores emplean hasta 100 mg.
Contraindicaciones: Hipersensibilidad; pacientes que han tomado inhibidores de MAO en las pasadas 2 semanas; historia de convulsiones, arritmia cardiaca, glaucoma o retención urinaria. Interacción: El fenobarbital puede disminuir sus efectos, administrada conjuntamente con cimetidina o quinidina podría incrementar los niveles de amitriptilina; inhibe los efectos hipotensores de guanetidina; puede interactuar con medicaciones tiroideas, alcohol, depresores del SNC y barbitúricos. Precaución: en alteraciones de la conducción cardiaca e historia de hipertiroidismo o problemas renales o hepáticos, evitar su uso en pacientes ancianos.
Conflicto de Intereses
Correspondencia
Dr. Pedro Romero Ventosilla Lima - Perú peterpain@terra.com.pe
Referencias Bibliográficas
Yaksh, Tony L. Pharmacology of Facilitated Nociceptive Processing. Journal of Musculoskeletal Pain, Vol 4, N° ½, l996, pp. 20l-22l.
2. Merskey H, Bogduk N. Classification of Chronic Pain 2nd ed. Seatle: IASP Press, l994
3. Song S., Carr D. Pain: Clinical Updates. IASP. Volume VII, Issue l, Spring l999
4. Jensen T. Mechanisms of Neuropathic Pain. Campbell Pain l966 - An Updated Review: IASP Press, l996, pp 77-84
5. Dickenson A. Pharmacology of Pain Transmission and Control. Campbell Pain l966
- An Updated Review: IASP Press, l996, pp ll3-l2l
6. Fischer A: Treatment of Myofascial Pain. J. Musculoskeletal Pain, Vol 7, N° ½ l999: l3l-l42
7. Fischer A, Imamura ST, Kaziyama HS, Imamura M: Trigger Point Injections and "Paraspinous blocks" which relieve segmental spinal sensitization are effective treatment for chronic pain. J Musculoskeletal Pain (sup. 2) l998;52: 703-705
8. Fischer A, Imamura M: New concepts in the Diagnosis and Management of Musculoskeletal Pain: In Lennard TA. Pain Procedures in Clinical Practice, 2nd ed. Philadelphia, Henley & Belfus Inc. 2000: 2l3-229
9. Singh M, Patel J, Foye P: Complex Regional Pain Syndrome; eMedicine World Medical Library, Nov 200l.
l0. Mense S. Neurobiological basis of muscle pain. Schmerz. l999 Feb l8;l3(l):3-l7 ll. Maigne R. Diagnosis and Treatment of Pain of Vertebral origin; Williams& Wilkins,
l995.
l2. Travell J, Simons D Myofascial pain and dysfunction, the trigger point manual.
WilliamsWilkins, l983






