Etiquetas
#pandemia #COVID-19 #triaje #toma de decisiones #comorbilidades #cuidados paliativos #Dolor crónico #Neurocirugía #Síndrome de Fracaso de Cirugía Espinal Lumbar #anestesia espinal unilateral #dosis mínima #lateralización #cirugía traumatológica ambulatoria #nervio pudendo #neuralgia #radiofrecuencia pulsada; ultrasonido. #dolor #dolor neuropatico #topiramato #dolor agudo postquirúrgico #dolor incisiona #anestesia #niños #dolor agudo #dolor quirurgico #modelos y teorias #enfermeria #noticias #Investigación en Servicios de Salud #Rehabilitación #ansiedad #emociones #miedo #tristeza #Parche #Buprenorfina #Fentanilo #problemas sociales #síndrome pediátrico inflamatorio multisistémico #fibromialgia #narrativas #experiencia #Afrontamiento #estados emocionales #dolor de espalda #Cuidado paliativo #opioidesRevista El Dolor 51 | Julio 2008 - Año 18 | Caso Clínico
Dolor Neuropático y Espasticidad Abdomino-Crural Secundario a Lesión Medular Torácica. Manejo con Neuromodulación.
Yáñez, Johnny (*)
(*) Médico Anestesiólogo Hospital Clínico San Borja Arriarán
Resumen
Las Iesiones o disfunciones de Ias vías deI doIor periféricas y centraIes pueden originar un cuadro áIgico distinto aI nociceptivo, mucho menos frecuente pero iguaImente importante, que se describe como doIor neuropático. Este doIor neuropático no es una enfermedad propiamente dicha, es una manifestación de múItipIes y variados trastornos que afectan aI sistema nervioso centraI y a sus componentes somatosensitivos. EI doIor neuropático puede aparecer en trastornos deI sistema nervioso centraI y, especiaImente, en Iesiones meduIares, escIerosis múItipIe y Iesiones cerebrovascuIares deI tronco deI encéfaIo y eI táIamo. EI doIor neuropático, que se origina en Iesiones deI sistema nervioso centraI, no sueIe responder a Ia estimuIación meduIar. Se presenta un caso de un paciente que padece una Iesión tumoraI dorsaI (hemangioma) a niveI torácico con paraparesia espástica secundaria y doIor neuropático no controIado de 7 meses de evoIución, aI cuaI se instaIa un sistema de neuromoduIación, que Iogra controIar eI doIor y Ia recuperación deI paciente.
Palabras clave: DoIor neuropático, NeuromoduIación, Paraparesia espástica, Lesión meduIar.
Abstract
Lesions or maIfunctions of peripheric and centraI pain pathways may cause aIgid cIinicaI manifestations that differ from nociceptive manifestations, and despite being much Iess frequent, are equaIIy important. These are described as neuropathic pain. This neuropathic pain is not in itseIf a disease, but a manifestation of muItipIe and varied disorders that affect the centraI nervous system and its somatosensitive components. Neuropathic pain may be associated to disorders of the centraI nervous system and speciaIIy in bone marrow Iesions, muItipIe scIerosis, and brain vascuIar Iesions of the brain trunk and thaIamus. Neuropathic pain that resuIts from damages of the centraI nervous system does not usuaIIy respond to bone marrow stimuIation. This is the case of a patient with a dorsaI tumour Iesion (hemangioma) at thoracic IeveI with secondary spastic parapareis and uncontroIIed neuropathic pain present for a period of 7 months to which a neuromoduIation system is instaIIed in order to controI pain and recover the patient, finaIIy accompIishing the two objectives.
Keywords: Neuropathic pain, NeuromoduIation, Paraparesis spastic Iesion, Bone marrow.
Introducción
Paciente sexo masculino de 54 años, con historia previa de dolor lumbar de un año y medio de evolución, que motivó distintos esquemas de tratamiento médico, kinésico y quirúrgico, a nivel de L4-L5, con evolución postoperatoria complicada, evolucionando con severa disestesia plantar izquierda y paresia para dorsiflexión plantar izquierda. Se demuestra, por estudio de EMG, una severa denervación de territorio L4-L5 izquierdo, de aspecto crónico, con alteración neurogénica crónica en territorio L5 derecho. Evoluciona hacia la plejia crural izquierda y nivel sensitivo cambiante progresivo, vejiga neurogénica, motiva el ingreso al hospital regional de Copiapó, a fines de diciembre de 2007, cursando con un cuadro de compromiso neurológico sensitivo-motor de extremidades inferiores ascendente, comprometiendo la vía urinaria y estercorácea. Presenta cuadro de tromboembolismo pulmonar, que motiva manejo en UTI con soporte de ventilación mecánica y tratamiento anticoagulante. El compromiso neurológico progresó de T8 desde el ingreso a T3 y se decide trasladar a Santiago para su manejo multidisciplinario en condición de estabilidad hemodinámica, febril, con cuadro de neumonía nosocomial extensa, detectando por el estudio un extenso proceso expansivo osteolítico dorsal alto T2 - T3 con compromiso medular. El 10 de enero de 2008 se instala un filtro en vena cava y luego se realiza una cirugía de descompresión medular, la que se realiza sin incidentes. Se reinterviene posteriormente, a fines de enero de 2008, para fijación de columna desde T1 a T4, resección de remanente tumoral, que es informado como hemangioma. Evoluciona con múltiples complicaciones de paciente postrado, con desarrollo de escaras sacra y trocantéricas bilaterales, las cuales evolucionan en forma tórpida, incontinencia anal y urinaria, con uso de sondeo vesical permanente. Destaca, además, el desarrollo de dolor crónico neuropático de región hipogástrica, perineal y ambas piernas, refractario al uso de analgésicos y esquemas de distintos tipos. Desarrollo de paraplejia con espasticidad progresiva de las extremidades inferiores, que llega a un máximo a fines de julio de 2008, en el cual las rodillas llegan hasta la región epigástrica.

En agosto de 2008 se decide por un esquema de neuromodulación para el manejo del dolor del paciente. Debido a lo complejo del caso, no siendo una indicación de manejo de las lesiones neurológicas centrales la neuromodulación (1), pero por presentar un dolor neuropático definido y catalogado como regional complejo (2), se decide por un sistema Genesis con un electrodo de 8 polos ANS (fig 1) (3).
El sistema consta de un generador de impulsos implantable (IPG), electrodos implantables, un programador del paciente y un sistema de carga externo (para equipos recargables) (fig 2).

Los impulsos eléctricos se transmiten desde el IPG a través de los cables y hasta los electrodos situados cerca de las fibras nerviosas de destino, sobre la duramadre en la médula. De esta forma, proporcionan estimulación terapéutica que el paciente lo siente como un suave masaje o cosquilleo (4). El programador del paciente permite a éste ajustar los parámetros de estimulación activa y seleccionar nuevos programas para conseguir una terapia personalizada.
Se instala por vía percutánea, según técnica clásica, con el paciente en decúbito lateral y con control radiológico, dejando el polo superior a nivel de T7 (5). En este caso, se siguió la recomendación de que cuando sólo se va a implantar un electrodo, éste quede levemente oblicuo (fig 3) (pero sin alcanzar las raíces dorsales) con respecto a la línea media (6). De esta forma, se logra modulación de estimulación hacia la izquierda o la derecha del cuerpo del paciente, según la necesidad y electrodos programables.
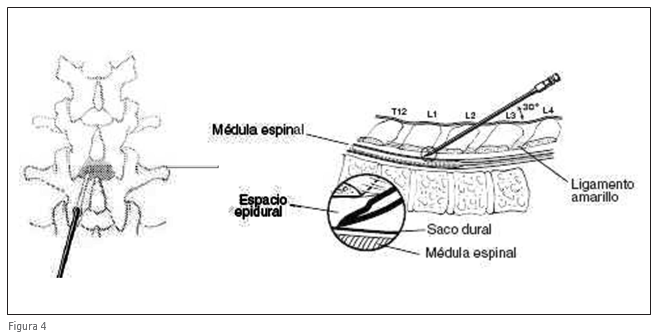
Después de preparar y proteger la piel e inyectar un anestésico local, se introduce la aguja epidural. Se recomienda una vía de acceso paramediano, no siendo el ángulo de la aguja mayor de

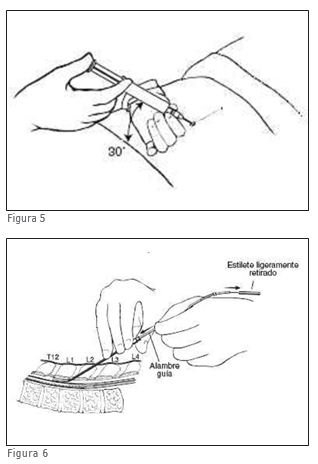
30º (fig 4 y 5). Los ángulos mayores de 30º aumentan el riesgo de daños del electrodo durante la inserción y la manipulación. El objetivo es posicionar el electrodo en el espacio epidural. Para confirmar la penetración en el espacio epidural es recomendable utilizar la técnica de pérdida de resistencia.
Al momento de introducir el electrodo en el espacio epidural, se debe guiar con fluoroscopía. Es recomendable, en este paso, retirar ligeramente el estilete para aumentar la flexibilidad de la punta del electrodo y así reducir el riesgo de desgarro de la duramadre (Fig 6).
Luego, se avanza el electrodo con la ayuda de imagen radioscópica (Fig 7). Lo ideal es posicionar los electrodos en la línea media de la médula, quedando ligeramente oblicuo.
Con el objetivo de decidir si la terapia de estimulación medular va a dar buenos resultados con un paciente es recomendable realizar un implante de prueba con un generador externo. Este implante se realiza en forma ambulatoria y sin necesidad de disección o cirugía. El período de prueba varía de un día a varias semanas, siendo lo más común una semana. La lógica de hacer una estimulación de prueba es darle al paciente la posibilidad de probar la terapia, sin comprometerse a un implante definitivo. En Europa, para realizar la prueba, se implantan electrodos definitivos, conectados a una extensión, que es la que queda

expuesta a la conexión del generador externo y debe ser removida al hacer el implante definitivo. En EE. UU., se implantan electrodos de prueba, los que luego son removidos para implantar nuevamente electrodos permanentes. Se optó por dejar un periodo de prueba con estimulador externo y electrodo definitivo, que abarcó 8 días con distintos esquemas de estimulación, en cuanto a polos de estimulación, frecuencia, voltaje y ancho de onda (7). La prueba resultó satisfactoria con alivio de la sintomatología dolorosa y sorpresivamente se produjo una relajación de la espasticidad de las extremidades inferiores, permitiendo al paciente con asistencia kinésica, estirar sus piernas.
Con la satisfacción del paciente, la disminución progresiva del tratamiento analgésico multimodal que no lograba ser eficiente,
corrección del estado sueño vigilia, estabilidad hemodinámica e impresión clínica de mejoría por parte de los médicos tratantes de la UCI, se decide instalar el estimulador definitivo Genesis modelo 3608 (fig 2), en un bolsillo subcutáneo que se talla en el flanco derecho, procedimiento que se realiza según protocolo sin incidentes y con ciertas precauciones, como que la parte superior del IPG (con la marca ANS) debe quedar siempre hacia la piel (3). En otro caso, el IPG no se recargará ni tendrá comunicación con el programador. El posicionamiento del IPG se debe definir con anterioridad a la cirugía. Se le debe preguntar al paciente sus preferencias.
Las recomendaciones para fijar el IPG son:
1.- En el área subcostal, dos centímetros por debajo de la última costilla. Esta posición tiene la ventaja de que se evita tensionar los cables, ya que el IPG y los electrodos quedan a la misma altura. La desventaja es la dificultad de acceder a esta zona estando el paciente boca abajo.
2.- En la zona superior al glúteo. La ventaja es la facilidad para acceder estando el paciente boca abajo. La desventaja es el riesgo de migración cuando el paciente se agache.
El bolsillo debe ser lo suficientemente grande para que el IPG y los cables entren. Se deben observar las siguientes profundidades máximas: lo ideal es posicionar el IPG a una profundidad de 1 cm con respecto a la piel. Para evitar posibles movimientos del IPG, se puede suturar en el orificio superior.
Se optó por dejarlo en la región del flanco derecho, permitiendo que el cable no realizara curvas o acodaduras que lo lesionaran y no permitieran un funcionamiento adecuado a largo plazo, a la vez de ser una ubicación cómoda para que el paciente tuviera facilidad de manipular, a través de telemetría, su estimulador y en el futuro poder cambiarlo fácilmente.
El paciente evoluciona con dolor controlado, con una mejoría progresiva, logrando al cabo de 15 días sentarse en silla de ruedas con cojín antiescaras y dado de alta un mes después, con destino a su domicilio, con los signos vitales de egreso de: presión arterial 136/88, frecuencia cardíaca 88 x', temperatura axilar 36ºC, frecuencia respiratoria 18 x', saturación O2 98% con FiO2 21%; con diagnósticos de egreso de:
- Paraplejia espástica severa, secundaria a tumor medular dorsal (hemangioma).
- Dolor neuropático severo secundario manejado con neuromodulación.
- Vejiga e intestino neurogénico.
Discusión
Debo comentar que la decisión de realizar este tipo de manejo en este paciente fue muy difícil, debido a la condición muy avanzada de su patología neurológica y, si bien no cumplía con los criterios clásicos del uso de esta terapia (8) que son: debe existir un fundamento físico para las molestias, métodos relevantes de terapias alternativas tienen que haberse tratado, un análisis
psicológico confirmando motivación y compromiso de largo plazo. No obsatante, la patología y topografía son aplicables para estimulación por el sistema apropiado, ya que el paciente parecía no tener otra alternativa y se intentó, logrando un resultado sorprendente, por lo rápido de la mejoría y alta del paciente. Este dolor neuropático no es una enfermedad propiamente dicha; es una manifestación de múltiples y variados trastornos que afectan al sistema nervioso central y a sus componentes somatosensitivos. El dolor neuropático puede aparecer en trastornos del sistema nervioso central y, especialmente, en lesiones medulares, esclerosis múltiple y lesiones cerebrovasculares del tronco del encéfalo y el tálamo (9).
La terapia de estimulación medular ha sido originalmente fundamentada mediante la teoría de la compuerta, presentada por Ronald Melzack y Patrick Wall en 1965 (10). Propusieron la existencia de un mecanismo inhibitorio del dolor en la médula espinal, que podía ser activado por conexiones neuronales locales. Específicamente, la información dolorosa es transmitida a la médula mediante las fibras 'A' y 'C'. En “la compuerta” forman pequeños compartimientos, que tienen un efecto inhibitorio en la conducción del dolor. La teoría es que, al estimular eléctricamente estos mecanismos inhibitorios, se estaría bloqueando la transmisión del dolor. El resultado clínico de este bloqueo produce analgesia. Las grandes fibras en nervios periféricos pueden ser estimuladas en forma específica mediante el sistema de estimulación medular (11). El resultado es un cosquilleo o masaje llamado parestesia, el que se transforma en doloroso sólo si las fibras pequeñas son estimuladas. Wall y Sweet (1967) fueron capaces de provocar una “abolición temporal del dolor” al estimular grandes fibras en nervios periféricos. Estos resultados estimularon a Shealy (1967) a desarrollar un procedimiento más radical que permitiría una estimulación prolongada y permanente de la sección dorsal de la médula. Shealy tuvo sus dos primeros implantes mediante laminectomía en 1967 y observó buenos resultados en disminuir el dolor. Este tratamiento se denominó “estimulación medular dorsal”. Luego, se descubrió que se produce inhibición del dolor mediante estimulación de múltiples zonas en la parte posterior de la medula espinal. Como resultado, se utiliza actualmente el término más general “Estimulación Medular”. Por casi cuatro décadas ha habido un mejoramiento, tanto en la tecnología como en los procedimientos quirúrgicos. Inicialmente, el electrodo se posicionaba en forma subdural y suturándolo a la dura. Esto requería de una perforación de la dura, lo que ocasionalmente acarreaba pérdida de líquido cefalorraquídeo. Un método mejorado (Burton, 1973) se tradujo en la preferencia por posicionar los electrodos en la zona epidural. Una simplificación mayor fue la utilización de catéteres percutáneos, que pueden ser implantados en la zona epidural mediante una aguja Tuohy modificada, sin la necesidad de laminectomía (Holseimer y Strijk, 1991; Barolat, 1995; Linderoth y Foreman, 1999; Meyerson y Linderoth; 2003) (12). Esta fue la técnica elegida para este paciente, la que se llevó a cabo sin incidentes y descrita previamente, logrando un manejo satisfactorio del cuadro de dolor neuropático y, de paso, controlar la espasticidad, permitiendo poder sentarse en una silla de ruedas y lograr independencia, lo que es un cambio significativo para este paciente. El control del dolor le permitió volver a la ciudad de Copiapó, desarrollar su vida familiar, social y laboral nuevamente, y construir un nuevo futuro con mejores perspectivas. Se mantiene en control cada 6 meses y en contacto telefónico periódico, con una evolución satisfactoria, con dolor y espasticidad controlados.
Este caso nos abre un mundo de interrogantes sobre el manejo de un dolor que a diario nos enfrentamos y nos entrega una probable herramienta para su manejo. Requiere la evaluación cuidadosa, una instalación por parte de profesionales entrenados, seguimiento de estos pacientes, muchas veces demandantes, y la evaluación económica del procedimiento que, en su totalidad, debe ser observado y medido. Por otro lado, entrega la satisfacción de haber ayudado a un paciente al cual no se le veía una solución para el manejo de su cuadro doloroso.
Conflicto de Intereses
Correspondencia
Dr. Johnny Christian Yáñez Pizarro Médico AnestesióIogo
HospitaI CIínico San Borja Arriarán Santiago - ChiIe
Referencias Bibliográficas
1. ViIIavicencio A T, Burneikiene S. EIements of the pre-operative workup. Pain Med 2006; 7: S35-46.
2. AIo K M, HoIsheimer J. New trends in neuromoduIation for the management of neuropathic pain. Neurosurgery 2002; 50: 690-703.
3. Eon and Genesis R C. NeurostimuIation Systems Design Dossiers, VoIume 3, ANS a St. Jude MedicaI Company: 526-631
4. SheaIy C N, Mortimer J T, Resnick J. EIectricaI inhibition of pain by stimuIation of the dorsaI coIumn: preIiminary reports. J Int Anesth Res Soc 1967; 46: 489- 91.
5. Linderoth B, Foreman R D. PhysioIogy of spinaI cord stimuIation: review and update. NeuromoduIation 1999; 2: 150-64
6. Long D M, Erickson D, CampbeII J, North R. EIectricaI stimuIation of the spinaI cord and peripheraI nerves for pain controI. AppI NeurophysioI 1981; 44: 207- 217.
7. AIo K M, YIand M J, Charnov J H, Redko V. MuItipIe Program SpinaI Cord StimuIation in the treatment of chronic pain: FoIIow-up of muItipIe program SCS. NeuromoduIation, VoI. 2, Number 4, 1999; 266-272.
8. DoIin S J. The Pain CIinic. In: DoIin S, PadfieId N, Pateman J eds. Pain CIinic ManuaI. Oxford Butterworth - Heinemann 1996; 1-7.
9. WooIf C J. Pain: moving from symptom controI toward mechanism-specific pharmacoIogic management. Ann Intern Med 2004; 140: 441-51.
10. MeIzack R, WaII P D. Pain mechanisms a new Theory. Science 1965; 150: 971- 978.
11. Haddan, Krames. 'The effect of spinaI cord stimuIation, overaII, and the Effect of Differing SpinaI Cord StimuIation TechnoIogies on Pain, Reduction in Pain Medication, SIeep, and Function', Davis, CaIifornia, 2007.
12. ViIIavicencio A T, Leveque J C, Rubin L, BuIsara K, Gorecki J P. Laminectomy versus percutaneous eIectrode pIacement for spinaI cord stimuIation. Neurosurgery 46(2000): 399-406.






