Etiquetas
#pandemia #COVID-19 #triaje #toma de decisiones #comorbilidades #cuidados paliativos #Dolor crónico #Neurocirugía #Síndrome de Fracaso de Cirugía Espinal Lumbar #anestesia espinal unilateral #dosis mínima #lateralización #cirugía traumatológica ambulatoria #nervio pudendo #neuralgia #radiofrecuencia pulsada; ultrasonido. #dolor #dolor neuropatico #topiramato #dolor agudo postquirúrgico #dolor incisiona #anestesia #niños #dolor agudo #dolor quirurgico #modelos y teorias #enfermeria #noticias #Investigación en Servicios de Salud #Rehabilitación #ansiedad #emociones #miedo #tristeza #Parche #Buprenorfina #Fentanilo #problemas sociales #síndrome pediátrico inflamatorio multisistémico #fibromialgia #narrativas #experiencia #Afrontamiento #estados emocionales #dolor de espalda #Cuidado paliativo #opioidesRevista El Dolor 68 | Diciembre 2017 - Año 27 | Originales
Relación entre el Adecuado Manejo del Dolor Agudo Perioperatorio e Incidencia de Dolor Crónico no Oncológico
Recibido: 03-08-2018Aceptado: 03-10-2018
Páginas 10-16
Romero, Camila (1); Contreras-Domínguez, Víctor (2); Contreras, Felipe (3); Carbonell-Bellolio, Paulina (4)
(1) Médico Residente de Anestesiología. Universidad de Concepción. Chile.
(2) Médico Anestesiólogo. Servicio de Urgencia y Anestesia Hospital Clínico Regional de Concepción. Chile.
(3) Interno de Medicina. Universidad San Sebastián. Concepción. Chile.
(4) Médico Anestesiólogo. Servicio de Urgencia Hospital Clínico Regional de Concepción. Chile.
Resumen
El adecuado manejo perioperatorio del dolor agudo y la elección de la técnica anestésica influyen en la incidencia de complicaciones a corto, mediano y largo plazo, encontrándose en este grupo el desarrollo de dolor crónico no oncológico (DCNO). Debido al aumento de la prevalencia de dolor crónico no oncológico y su relación con un manejo inadecuado o insuficiente del dolor agudo en el periodo perioperatorio, hemos realizado una revisión de su fisiopatología, los factores de riesgo y las técnicas preventivas que permitirían mitigar y/o disminuir su incidencia.
Palabras clave: dolor crónico, dolor agudo, dolor quirúrgico.
Abstract
The adequate perioperative management of acute pain and the correct choice of the anesthetic technique influence the incidence of complications in the short, medium and long term, being in this group the development of chronic non-oncological pain (CNOP). Due to the increase in the prevalence of non-oncological chronic pain and its relation with an inadequate or insufficient management of acute pain in the perioperative period, we have carried out a review of its pathophysiology, risk factors and preventive techniques that would allow mitigating and/or decrease its incidence.
Keywords: chronic pain, acute pain, surgical pain.
Introducción
El dolor crónico no oncológico (DCNO) es un desafío para los equipos de salud y muy particularmente para los anestesiólogos. En la actualidad, aproximadamente el 10% de los pacientes pueden desarrollar DCNO con relación a distintos tipos de cirugía (1). Se asocia, en la gran mayoría de los casos, a cirugías cruentas y/o de gran envergadura, tales como: cirugías de amputación de extremidades, de tórax abierto (toracotomía), de mama, de pared abdominal, cardíaca, cesáreas y la colecistectomía abierta, entre otras (2).
La cirugía es reconocida como una de las causas más frecuentes de dolor crónico en pacientes que asisten a clínicas del dolor. En una encuesta realizada a más de 5.000 pacientes, se encontró que el grupo de mayor incidencia (34,2%) estaba asociado a enfermedades degenerativas. El segundo grupo más numeroso (22,5%) había desarrollado DCNO como consecuencia de alguna cirugía (3).
Habitualmente, el DCNO es definido como aquel dolor que persiste por más de 3 meses tras una cirugía. Esta es una complicación reconocida en varias cirugías habituales y pueden llegar a ser una complicación seria a largo plazo, como ocurre en la reparación de hernia inguinal (4). El DCNO tiene un alto y negativo impacto en la calidad de vida y actividades cotidianas de los pacientes afectados por éste; pero también, existe un alto costo para la sociedad en relación a los gastos asociados en salud y sistema de previsión.
Fisiopatología
El trauma y la inflamación que ocurren por la manipulación de tejidos y las incisiones durante la cirugía activan nociceptores y se traducen en impulsos eléctricos que van a la médula espinal, a través de las vías aferentes primarias Aδ y C. La primera neurona aferente hace sinapsis con la segunda neurona en el asta dorsal de la médula y lleva el impulso a centros superiores, a través de la vía espinotalámica contralateral y espinoreticular, que son las dos vías ascendentes principales. A nivel central, existen múltiples proyecciones a la corteza cerebral y otros centros, los que traducen estos impulsos en dolor. El dolor inflamatorio ocurre porque se liberan mediadores inflamatorios y sensibilizadores como las citoquinas, bradiquininas y prostaglandinas, desde las células lesionadas en el sitio de daño tisular.
Los nociceptores han demostrado plasticidad reversible en respuesta a los mediadores inflamatorios. El umbral de activación de los nociceptores disminuye, lo que aumenta la sensibilidad al dolor en el sitio de la lesión tisular (sensibilización periférica).
Este tipo de dolor inflamatorio, secundario a la estimulación local, habitualmente se detiene una vez que la fuente de los mediadores cede, a medida que la cicatrización ocurre o la patología es controlada. La sensibilidad aumentada puede contribuir a la curación al ayudar a proteger la parte del cuerpo dañada hasta que se haya producido una reparación. El sistema nervioso central también demuestra plasticidad en respuesta al dolor y se puede potenciar la señalización del dolor dentro de la médula espinal.
Con la entrada nociceptiva continua, la relación estímulo- respuesta se altera y puede ocurrir un aumento en la excitabilidad de las neuronas en el sistema nervioso central, conocida como sensibilización central. Clínicamente, se manifiesta como una respuesta aumentada al estímulo doloroso (hiperalgesia), y como dolor secundario a estímulo no doloroso (alodinia).
El reclutamiento, la potenciación a largo plazo y la hiperalgesia secundaria son todos procesos asociados con la sensibilización central. El reclutamiento ocurre con la activación repetida de fibras C y se debe a la acción del glutamato en los receptores N-metil-D-aspartato (NMDA). Bajo condiciones normales, un ion magnesio bloquea el receptor NMDA. Con el estímulo doloroso, el ion magnesio que bloquea es removido y la respuesta al estímulo doloroso de las segundas neuronas es amplificada. Esto explica por qué los antagonistas de los receptores NMDA, como la ketamina, sirven para atenuar o bloquear el reclutamiento. La respuesta de las segundas neuronas puede durar más que el estímulo inicial y esto es conocido como potenciación a largo plazo, que contribuye a la hiperalgesia. Una disminución del umbral del dolor fuera del área de inflamación (hiperalgesia secundaria) ocurre por una activación aumentada de las segundas neuronas en el asta dorsal de la médula espinal.
El daño neuronal juega un rol importante en el desarrollo del DCNO. Siguiendo la injuria neuronal, ocurren descargas ectópicas de nervios dañados y no dañados, lo que lleva a dolor espontáneo. El aumento de la entrada nociceptiva en el asta dorsal contribuye a la sensibilización central. La pérdida de interneuronas inhibitorias en el asta dorsal produce una desinhibición de las vías del dolor y la facilitación de la transmisión del dolor (5).
El proceso de sensibilización central se considera importante para el desarrollo de dolor persistente; por lo tanto, las técnicas quirúrgicas e intervenciones farmacológicas para minimizar la sensibilización central son un área de gran interés.
Factores de riesgo
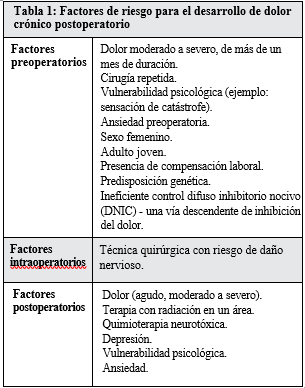
Existen diversos factores de riesgo que han sido identificados para el desarrollo de DCNO. Algunos de éstos, como la predisposición genética y el género, no son modificables; sin embargo, es posible reducir el riesgo al considerar otros factores, tales como el abordaje quirúrgico, el manejo del dolor agudo y la vulnerabilidad psicológica (Tabla N° 1).
Control del estrés pre operatorio
En búsqueda de técnicas eficientes para el manejo adecuado de la ansiedad preoperatoria, nos parece interesante analizar algunas intervenciones no farmacológicas del tipo enseñanza/ aprendizaje, tales como preparación psicológica, relajación, hipnosis, escucha de música, intervención centrada en la emoción, información sensorial, técnicas de distracción, etc. En general, se sabe que éstas pueden ser una alternativa eficiente a la administración de medicamentos ansiolíticos para disminuir la ansiedad preoperatoria. Es muy importante tener en cuenta la preferencia del paciente, la experiencia del personal de salud y los recursos disponibles.
La ansiedad preoperatoria, más allá de los efectos emocionales en el paciente, también puede tener repercusiones negativas en la cirugía, incluyendo estadía hospitalaria prolongada (6). Dado el amplio impacto de la ansiedad preoperatoria, es fundamental identificarla y disminuirla en el periodo pre quirúrgico.
Los efectos de la preparación psicológica, tales como: información procedimental, información sensorial, intervención cognitiva, relajación, hipnosis y la intervención centrada en la emoción en pacientes sometidos a cirugía electiva bajo anestesia general sobre los resultados postoperatorios como el dolor, recuperación del comportamiento, duración de la estancia y afecto negativo, fueron estudiados por Powell R y cols. (7). Ellos realizaron un meta-análisis que incluyó
105 estudios (10.302 participantes). Los participantes se sometieron a una amplia gama de procedimientos quirúrgicos, y se utilizó una gama de componentes psicológicos en las intervenciones, con frecuencia en combinación. Sólo en 38 de los 105 estudios existían datos confiables y pruebas estadísticas con la robustez suficiente, como para hacer confiable sus conclusiones. En general, los autores califican la calidad de la evidencia para cada resultado como “baja” y “muy baja”, debido al alto nivel de heterogeneidad en los estudios meta- analizados y el riesgo poco claro de sesgo. Actualmente, la evidencia es insuficiente para llegar a conclusiones firmes sobre el papel de la preparación psicológica para la cirugía. Se necesitan más análisis para explorar la heterogeneidad en los datos, para identificar más específicamente cuándo las técnicas de intervención son beneficiosas. Como la calidad actual de la evidencia es baja o muy baja, existe la necesidad de realizar investigaciones bien conducidas y claramente informadas.
Un estudio realizado por Ko YL y cols. (8) investigó el efecto de la audición de una cinta de audio de relajación sobre los niveles de ansiedad en 80 pacientes con cirugía electiva. Se realizaron pruebas antes y después que los pacientes escucharan las cintas. El cuestionario de ansiedad STAI, la respiración, el pulso y la presión arterial se utilizaron para medir nivel de ansiedad. Después que los pacientes escucharon la cinta de relajación, su tasa de respiración disminuyó, la frecuencia cardíaca también cayó, la presión arterial sistólica disminuyó y la puntuación del STAI también disminuyó. Todos mostraron un nivel significativo de diferencia (p <0,05). La mayoría de los pacientes escucharon la cinta durante toda la estancia hospitalaria (66,3%), y la puntuación STAI pudo reducirse aún más al aumentar el número de sesiones de escucha (p <0,001). Los resultados muestran que una cinta de audio de relajación puede reducir significativamente el nivel de ansiedad y signos vitales relacionados con la ansiedad en pacientes pre quirúrgicos. Se recomienda que las cintas de relajación se incluyan en el estándar de atención para aliviar la ansiedad en los pacientes quirúrgicos.
La utilidad de la hipnosis para el control del dolor y la ansiedad fue estudiada en pacientes beneficiarios de una ecografía transrectal para la biopsia de próstata por Hizli F y cols. (9). Se incluyeron 64 pacientes para la biopsia eco-guiada de próstata, asignados aleatoriamente para recibir una sesión de hipnosis pre quirúrgica de 10 minutos (n = 32, edad media 63,5
± 6,1, p = 0,289) o una sesión de control pre quirúrgico (n = 32, edad 61,8 ± 6,8, p = 0,289). La sesión de hipnosis incluyó sugerencias para aumentar la relajación y reducir la ansiedad. El dolor y la ansiedad de la cirugía se midieron usando escalas analógicas visuales (EVA), Beck Anxiety Inventory (BAI) y Hamilton Ansiedad Scale (HAS), respectivamente. Después de la intervención, y antes de la cirugía, los pacientes en el grupo de hipnosis tenían valores medios significativamente inferiores para la VAS prequirúrgica [media 1 (0-8); P = 0,011], BAI (6,0 frente a 2,0, p <0,001) y HAS (11,0 frente a 6,0; p <0,001). Los resultados del estudio indican que una breve intervención de hipnosis antes de la cirugía puede ser eficaz para controlar la ansiedad prequirúrgico y, por tanto, el dolor, en pacientes que esperan dicha cirugía diagnóstica. En otro ensayo clínico aleatorizado (10), se estudió la utilidad de una breve sesión de hipnosis para reducir el trastorno psicológico prequirúrgico en 90 pacientes a las que se les efectuó una biopsia de mama. A un grupo se realizó una sesión de hipnosis pre quirúrgica de 15 minutos (n= 49) y sugerencias para una mayor relajación y disminución de la angustia. Al grupo control una sesión de control de atención quirúrgica de 15 minutos (n= 41), con escucha empática no directiva. La angustia preoperatoria se midió usando las escalas análogas visuales (VAS) y la versión corta del perfil de estados del humor (SV-POMS). Los pacientes del grupo hipnosis tuvieron valores medios significativamente inferiores para el colapso emocional de la VAS previa a la cirugía (p <0,0001), estado de ánimo depresivo del VAS (p
<0,02), y la ansiedad de SV-POMS (p <0,0001); como a la vez, niveles significativamente más altos para la relajación del VAS (p <0,001) que las pacientes del grupo control. Los resultados del estudio indican que una breve intervención de hipnosis antes de la cirugía puede ser un medio eficaz de controlar la angustia prequirúrgica en mujeres que esperan la cirugía diagnóstica de cáncer de mama.
Bradt y cols. (11) en una revisión sistémica analizan los efectos de la música con atención preoperatoria estándar versus atención estándar sola sobre la ansiedad preoperatoria en pacientes quirúrgicos. Se incluyeron 26 ensayos (2.051 participantes). Todos los estudios usaron la escucha de música grabada previamente. Los resultados indicaron que la escucha de música dio lugar, en promedio, a una reducción de la ansiedad de 5,72 unidades más (IC del 95%: -7,27 a -4,17; p < 0,00001) que la del grupo de atención estándar según lo medido con el Stait-Trait Anxiety Inventory (STAI-S), y de
-0,60 unidades estandarizadas (IC del 95%: -0,90 a -0,31; p < 0,0001). Se concluye que la escucha de música puede tener un efecto beneficioso sobre la ansiedad preoperatoria.
Labrague y cols. (12), en un ensayo clínico prospectivo y aleatorizado en 97 mujeres beneficiarias de una cirugía ginecológica, estudiaron la utilidad de la música para disminuir el estrés preoperatorio. 49 fueron asignadas al grupo control (grupo sin música) y 48 fueron asignadas al grupo experimental (grupo de música). La ansiedad preoperatoria se midió utilizando el STAI, y los signos vitales: presión arterial, pulso y respiración, fueron monitorizados de manera no invasiva. Las mujeres que escucharon música presentaron puntuaciones más bajas en el STAI, presión sistólica y diastólica que las del grupo de control. Se apoya el uso de la música durante el período preoperatorio para reducir la ansiedad y los síntomas desagradables en las mujeres sometidas a cirugía ginecológica.
Hace una década, Muzzarelli y cols. (13) estudiaron en 118 pacientes el uso de la aromaterapia para reducir la ansiedad antes de una colonoscopía programada o endoscopía digestiva alta. Se utilizó el STAI para evaluar los niveles de ansiedad antes y después de la terapia. El grupo control recibió un aceite inerte (placebo) para inhalación, y el grupo experimental recibió un aceite esencial de lavanda para inhalación. No hubo diferencias en los niveles de ansiedad entre la inhalación pre y post placebo en el grupo control. No hubo diferencias estadísticas en los niveles de ansiedad de estado entre la inhalación de aceite de lavanda pre y post en el grupo experimental. Este estudio demostró que la aromaterapia no fue eficaz.
Factores de riesgo quirúrgico y prevención
La técnica quirúrgica es un factor de riesgo reconocido en DCNO y es probable que la injuria nerviosa cumpla un rol (1). Muchas de las cirugías asociadas con el desarrollo de dolor crónico involucran nervios mayores en el campo quirúrgico, por ejemplo, en cirugía de mama (nervio intercostobraquial) y cirugía torácica (nervios intercostales). El daño nervioso debería ser minimizado para reducir el desarrollo de dolor crónico (14). La cirugía laparoscópica puede reducir el riesgo de daño nervioso intraoperatorio. Por ejemplo, existe evidencia de una menor incidencia de dolor persistente luego de una reparación de hernia por vía laparoscópica (4). Mujeres sometidas a cirugía por cáncer de mama en unidades con gran número de pacientes y por cirujanos experimentados, también presentan menor incidencia de dolor crónico y se piensa que esto se debe a la técnica quirúrgica y al menor daño nervioso. Muchas cirugías no incluyen la sección de troncos nerviosos, pero la injuria también puede ocurrir por estiramiento y aplastamiento de los nervios durante la tracción o la incisión de la piel, víscera (s), fascia (s), músculo (s) y articulaciones; debido a que todas las estructuras recién mencionadas están inervadas por nervios sensitivos. Sin embargo, es evidente que otros factores distintos a la injuria nerviosa son una causa importante de dolor crónico. La sección nerviosa intraoperatoria no siempre resulta en dolor neuropático y evitar la sección nerviosa no necesariamente previene el dolor crónico (15). La duración de la cirugía influye en el desarrollo de dolor crónico, siendo las cirugías de más de 3 horas las asociadas a mayor riesgo (16). Lo anterior puede reflejar patologías más complejas y con mayor grado de daño de tejido en el intraoperatorio.
Mientras que la cirugía habitualmente está indicada o es apropiada, hay situaciones donde es innecesaria y potencialmente inútil. La posibilidad de desarrollar DCNO debería ser considerada con la indicación quirúrgica. El dolor crónico es un problema reconocido luego de una cirugía estética como el aumento mamario y las pacientes deberían ser informadas del riesgo (17). En pacientes con dolor abdominal y síndromes de hiperalgesia visceral sin causa evidente del dolor pese a múltiples estudios debiera considerarse como una eventual causa de su padecer a la(s) potencial(es) noxa(s) secundarias al acto quirúrgico.
Anestesia regional y consideraciones analgésicas
Considerando los mecanismos fisiopatológicos propuestos que contribuyen al DCNO, parecería lógico suponer que el manejo adecuado del dolor perioperatorio será un beneficio a largo plazo en reducir la sensibilización central.
Anestesia regional
Las técnicas de anestesia regional usan anestésicos locales para bloquear la conducción de impulsos a través de los nervios. Al minimizar la transmisión de señales hacia o a través de la médula espinal, puede ser posible prevenir la entrada de impulsos nociceptivos hacia el asta dorsal de la médula y así prevenir la sensibilización central. Las técnicas espinal y epidural actúan a nivel de las raíces nerviosas, mientras que los bloqueos de nervio periférico, bloqueos de plexo e infiltración de la herida operatoria, interrumpen los impulsos de nervios periféricos. Una reciente revisión sistémica describió los beneficios de la analgesia peridural en las toracotomías al reducir el riesgo de dolor crónico a los 6 meses, y para los bloqueos paravertebrales al reducir el dolor crónico relacionado con la cirugía de cáncer de mama a los 5-6 meses (18). La anestesia espinal también ha demostrado ser beneficiosa en comparación con la anestesia general al reducir el riesgo de DCNO luego de una operación cesárea (19).
La amputación de alguna extremidad se asocia a un alto riesgo de DCNO. La injuria nerviosa es inevitable, sin embargo, la analgesia epidural perioperatoria reduce la incidencia de síndrome de miembro fantasma severo (20). Aunque existe alguna evidencia de los beneficios de técnicas de anestesia regional para reducir el DCPNO, no está completamente dilucidado si ésta aplica a todos los procedimientos.
Analgesia preventiva
El momento óptimo y modo de administración de anestesia perioperatoria regional y sistémica es aún debatido. La analgesia preventiva es administrada previamente a la incisión quirúrgica. La analgesia epidural preventiva tiene beneficios significativos en el dolor postoperatorio (20), sin embargo, el beneficio de otros tipos de analgesia preventiva no está tan claro (21).
La analgesia preventiva describe un tratamiento analgésico que excede su duración esperada. Puede ser importante para reducir el DCNO, al disminuir la sensibilización central. Se estima que para que un manejo analgésico sea efectivo en prevenir la sensibilización del sistema nervioso, debería actuar durante el periodo de tiempo en el que existe un estímulo inflamatorio, no solo la incisión de la piel, sino que más bien en todo el periodo postoperatorio. En una revisión sistémica efectuada por McCartney y cols., se evidenció que los antagonistas NMDA administrados en el periodo perioperatorio son eficientes en producir analgesia preventiva, y se piensa que se debe a prevenir la sensibilización central (22).
Ketamina
La ketamina es un antagonista del receptor NMDA y es a través de este mecanismo que previene la supresión mediada por receptores NMDA. También produce analgesia a través de la activación de las vías inhibitorias del dolor monoaminérgica descendentes y previene la hiperalgesia inducida por opioides (un aumento paradójico de la sensibilidad al estímulo doloroso en pacientes que reciben opioides) y la tolerancia aguda a opioides. La ketamina es raramente usada como anestésico único, debido a sus efectos adversos, pero puede ser muy útil como droga coadyuvante en pacientes que requieren altas dosis de opioides. Potencia la analgesia de los opioides, mejora el control del dolor y reduce los efectos secundarios asociados a los opioides (23). Ha sido administrada en bolo único y en dosis bajas (0,15-0,5 mg/kg); o bien, como bolo en dosis bajas, seguido de una infusión continua también a dosis bajas (2 a 4 mcg/kg/min) en pacientes sin tratamiento previo con opioides que son sometidos a una variedad de cirugías. La mayoría de los estudios muestran una reducción en los requerimientos de opioides postoperatorios y en el dolor principalmente en las primeras 24 horas, aunque algunos estudios también muestran beneficios a largo plazo (24). La analgesia epidural perioperatoria combinada con la ketamina endovenosa, reduce la hiperalgesia y el dolor crónico luego de cirugía colónica en comparación con la analgesia endovenosa sola (25)
Gabapentinoides
La gabapentina fue inicialmente introducida como un medicamento anticonvulsivante en los años 90. Estudios posteriores han mostrado sus beneficios en el tratamiento de dolor neuropático (26). Actúa en la subunidad presináptica α-2-δ de los canales de calcio presinápticos, inhibiendo el influjo de calcio y como consecuencia la liberación de neurotransmisores excitatorios de las vías del dolor (27). La pregabalina es estructuralmente similar a la gabapentina y tiene mayor potencial analgésico y un perfil farmacocinético más favorable en relación con la gabapentina.
Diversos estudios clínicos prospectivos aleatorizados han demostrado el beneficio del uso preventivo de gabapentina para reducir el dolor postoperatorio (28, 29). Recientemente, una revisión sistemática y metaanálisis, analizó el uso perioperatorio de gabapentina y pregabalina sobre el desarrollo de DCNO. Se evidenció un efecto positivo en pacientes que recibieron gabapentina en 4 de 6 estudios incluidos en este metaanálisis. Asimismo, la gabapentina demostró disminuir importantemente la incidencia de DCNO. En otra revisión sistémica y metaanálisis, se analizaron 3 estudios en los que se utilizó pregabalina; en todos ellos se evidenció un efecto analgésico preventivo. A la vez, en cuatro de seis estudios que analizaban los resultados funcionales a largo plazo, revelaron beneficios en el uso de gabapentina y pregabalina. Este análisis provee evidencia en que la administración perioperatoria de estos fármacos puede estar relacionada con la disminución de la incidencia del DCNO (30). Sin embargo, existe un número limitado de estudios en esta revisión, y esto, asociado a un cierto grado de sesgo en la publicación, hace necesario que se realicen estudios futuros bien diseñados para dilucidar el verdadero rol de la gabapentina y pregabalina en la prevención del DCNO.
Lidocaína endovenosa
En un reciente metaanálisis sobre el uso intraoperatorio de lidocaína endovenosa, Vigneault y cols. (31) encontraron una reducción del dolor agudo postoperatorio, mostrando mayores beneficios en aquellos pacientes sometidos a cirugía abdominal. Las administraciones sistémicas de anestésicos locales también han demostrado un efecto anti- hiperalgésico que dura por días luego de la cirugía, mucho después de la acción anestésica local del medicamento. El mecanismo de acción no está completamente dilucidado y no puede ser explicado por el bloqueo de los canales de sodio (32). Sin embargo, estos hallazgos sugieren que la lidocaína podría tener un papel en la prevención de la sensibilización central y, por lo tanto, un rol como analgésico preventivo e influenciar de este modo la incidencia del DCNO.
Factores psicosociales
La experiencia del dolor es más que la detección de un estímulo transmitido al sistema nervioso central. La percepción del dolor está influenciada por el estado anímico, la memoria, la expectación y ambiente social; es así, como los factores psicosociales deberían ser considerados en la evaluación del dolor y su manejo.
El modelo de evitación de miedo, que se considera importante en la iniciación y mantención del dolor crónico, demuestra la importancia de los factores psicológicos. En este modelo, una persona cree que el dolor indica peligro o daño. El miedo al dolor conduce a evitar actividades que puedan inducir o exacerbar el dolor. El comportamiento de evitación de miedo puede conducir al desuso y la discapacidad (33) y se ha evidenciado que el miedo al dolor predice mejor la discapacidad que el dolor en sí mismo (34). Las personas con pensamientos catastróficos son más propensas a entrar en este ciclo de comportamiento de evitación del miedo. El pensamiento catastrófico puede describirse como una evaluación negativa habitual casi inmediata de una situación. Una persona puede creer, por ejemplo, que si se dobla la espalda se romperá y se convertirá en usuario de silla de ruedas. La relación entre la experiencia del dolor y la actividad conductual está mediada por la expectativa de dolor y la anticipación de consecuencias catastróficas si se llevan a cabo ciertas actividades (35). La anticipación del dolor debe ser una respuesta útil y adaptativa que lleve a la modificación del comportamiento para evitar el dolor. Sin embargo, puede volverse inadaptable en el contexto del dolor crónico. Los estudios de neuroimagen que analizan cómo la anticipación y la ansiedad pueden aumentar la percepción del dolor han revelado que ciertas regiones son importantes para amplificar la experiencia del dolor. Estas regiones incluyen el complejo entorrinal, la amígdala, la corteza insular anterior y la corteza prefrontal (36).
Los factores psicológicos juegan un papel importante tanto en el dolor de espalda agudo como crónico, y en la transición del dolor agudo al crónico. De hecho, es conocido que los factores psicosociales tienen un mayor impacto que los factores biomédicos o biomecánicos en la discapacidad del dolor de espalda (37). A su vez, los factores psicológicos influyen en el dolor postoperatorio agudo. Por ejemplo, Katz y cols. (38) describieron una correlación entre la ansiedad preoperatoria y el dolor postoperatorio agudo en mujeres sometidas a cirugía de cáncer de mama.
En la literatura existe menos información sobre el papel de los factores psicosociales en el dolor persistente después de la cirugía; en contraste, la vulnerabilidad psicológica (por ejemplo, pensamiento catastrófico), la ansiedad, la depresión y el regreso tardío al trabajo, han demostrado ser importantes factores de riesgo (20, 39). Los pacientes con miedo a las consecuencias a largo plazo de la cirugía también presentan un mayor riesgo de dolor a largo plazo y una recuperación deficiente (40).
Dar sentido al dolor, lo que puede significar y lo que no significa es esencial para un afrontamiento efectivo. Las intervenciones cognitivas y conductuales preventivas disminuyen la ansiedad antes y después de la cirugía, reducen la intensidad del dolor postoperatorio y el uso de analgésicos (41). Un estudio de Egbert y cols. (42), que data de casi 50 años, demostró una reducción en los requerimientos de morfina y la duración de la estadía cuando a los pacientes se les proporcionó información preoperatoria sobre probables tratamientos postoperatorios y molestias e instrucciones sobre técnicas de relajación. Cuando los pacientes reciben información sobre lo que deberían esperar sentir, además a la información de procedimiento, experimentan menos dolor y angustia en comparación con cualquier tipo de información dada por sí sola (43). Relacionado esto, con el modelo de evitación de miedo, podemos ver que la información puede proporcionar la seguridad de que las sensaciones experimentadas después de un procedimiento son normales y no amenazantes. Por ejemplo, después de un reemplazo total de rodilla, se alienta a los pacientes a movilizarse a las pocas horas de la cirugía. Esto puede ser incómodo, pero es importante que a los pacientes se les asegure que el dolor no es igual al daño, que es normal sentir cierta incomodidad y no significa que se esté poniendo en peligro su intervención o que algo anda mal. Educar a los pacientes y sus cuidadores sobre el dolor fomentan una actitud más positiva para el alivio del dolor y, cuando sea posible, tratar de involucrar a los pacientes en su estrategia de control del dolor tiene especial importancia. A través de la participación activa, los pacientes desarrollan un mayor sentido de autoeficacia con respecto al tratamiento y comportamientos relacionados con la enfermedad y es más probable que cumpla con las decisiones de manejo alcanzadas (44). Los pacientes que responden pasivamente al dolor muestran mayor angustia e incapacidad, en comparación con aquéllos que intentan resolver el problema. Tener cierto control sobre la causa del dolor o el método de analgesia tiene un efecto beneficioso. Las relaciones sociales también pueden influir en el informe del dolor y la discapacidad. Un estudio de pacientes con dolor de espalda crónico descubrió que cuando hay una pareja presente que está atenta y puede ayudarlos a evitar actividades que pueden exacerbar el dolor, es probable que el paciente informe más dolor y rinda menos en las tareas. Las expresiones de dolor son reforzadas por el compañero que actúa para aliviar la actividad conductual del paciente, y esto se refleja en el aumento del nivel de dolor (35).
El manejo de las expectativas se reconoce como un componente importante de los programas de recuperación mejorados. Se espera que la información cuidadosamente presentada de cirujanos, anestesiólogos y enfermeras sobre el procedimiento quirúrgico, las experiencias sensoriales anticipadas, el tratamiento analgésico y el periodo de recuperación reduzcan la ansiedad y promuevan la recuperación (45). Al abordar estos problemas en el período perioperatorio es posible que podamos influenciar en reducir la progresión a dolor persistente y discapacidad en aquellos pacientes con factores de riesgo.
Conclusión
Al comprender los procesos fisiológicos que contribuyen al dolor persistente, podemos usar intervenciones terapéuticas para minimizar la progresión del dolor agudo al crónico. El conocimiento de los factores de riesgo para el desarrollo de dolor crónico postoperatorio puede ayudar a identificar a aquellos pacientes en alto riesgo y dirigir las intervenciones. Siempre se debe considerar el impacto de los factores psicológicos en la experiencia del dolor y se recomienda un enfoque de colaboración que involucre a los pacientes en sus decisiones de tratamiento para que experimenten el mejor resultado.
Conflicto de Intereses
Autor (es) no declaran conflicto de interés en el presente trabajo:
Recibido el 03 de Agosto 2018, aceptado para publicación el 03 de octubre 2018.
Correspondencia a:
Dr. Víctor Contreras-Domínguez Hospital Clínico Regional de Concepción Concepción. Chile.
Email: dr.vcontreras@gmail.com
Referencias Bibliográficas
(1) Kehlet H, Jensen TS, Woolf CJ. Persistent postsurgical pain: risk factors and prevention. Lancet 2006; 367:1618–1625.
(2) Schug SA, Pogatzki-Zahn EM. Chronic pain after surgery or injury. IASP. Clinical Updates 2011;XIX.
(3) Crombie IK, Davies HTO, Macrae WA. Cut and thrust: antecedent surgery and trauma among patients attending a chronic pain clinic. Pain 1998; 76:167–71.
(4) Jenkins JT, O’Dwyer PJ. Inguinal hernias. BMJ 2008;336:269–72.
(5) Reddi D, Curran N. Postgrad Med J 2014; 90:222–227.
(6) Wilson CJ, Mitchelson AJ, Tzeng TH, El-Othmani MM, Saleh J, Vasdev S, LaMontagne HJ, Saleh KJ. Caring for the surgically anxious patient: a review of the interventions and a guide to optimizing surgical outcomes. Am J Surg. 2016 Jul; 212(1):151-9.
(7) Powell R, Scott NW, Manyande A, Bruce J, Vögele C, Byrne-Davis LM, Unsworth M, Osmer C, Johnston M. Psychological preparation and postoperative outcomes for adults undergoing surgery under general anaesthesia. Cochrane Database Syst Rev. 2016 May 26; (5):CD008646.
(8) Ko YL, Lin PC. The effect of using a relaxation tape on pulse, respiration, blood pressure and anxiety levels of surgical patients. J Clin Nurs. 2012 Mar; 21(5-6):689-97.
(9) Hizli F, Özcan O, Selvi I, Eraslan P, Kösus A, Bas O. The effects of hypnotherapy during transrectal ultrasound-guided prostate needle biopsy for pain and anxiety. Int Urol Nephrol. 2015 Nov; 47(11):1773-7.
(10) Schnur JB, Bovbjerg DH, David D, Tatrow K, Goldfarb AB, Silverstein JH, Weltz CR, Montgomery GH. Hypnosis decreases presurgical distress in excisional breast biopsy patients. Anesth Analg. 2008 Feb; 106(2):440-4.
(11) Bradt J, Dileo C, Shim M. Intervenciones con música para la ansiedad preoperatoria. Cochrane Database of Systematic Reviews 2013 Issue 6. Art. No.: CD006908. DOI: 10.1002/14651858.
(12) Labrague LJ, McEnroe-Petitte DM. Influence of Music on Preoperative Anxiety and Physiologic Parameters in Women Undergoing Gynecologic Surgery. Clin Nurs Res. 2016 Apr; 25(2):157-73.
(13) Muzzarelli L, Force M, Sebold M. Aromatherapy and reducing preprocedural anxiety: A controlled prospective study. Gastroenterol Nurs. 2006 Nov-Dec; 29(6):466-71.
(14) Katz J, Seltzer Z. Transition from acute to chronic postsurgical pain: risk factors and protective factors. Expert Rev Neurother 2009; 9:723–44.
(15) Macrae WA. Chronic post-surgical pain: 10 years on. Br J Anaesth 2008; 101:77–86.
(16) Peters ML, Sommer M, de Rijke JM, et al. Somatic and psychologic predictors of long-term unfavorable outcome after surgical intervention. Ann Surg 2007; 245:487–94.
(17) Von Sperling ML, Høimyr H, Finnerup K, et al. Persistent pain and sensory changes following cosmetic breast augmentation. Eur J Pain 2011; 15:328–32.
(18) Andreae MH, Andreae DA. Local anaesthetics and regional anaesthesia for preventing chronic pain after surgery. Cochrane Database of Systematic Reviews 2012 ;(10).
(19) Nikolajsen L, Sørensen HC, Jensen TS, et al. Chronic pain following Caesarean section. Acta anaesthesiol Scand 2004; 48:111–16.
(20) Macinytre PE, Schug SA, Scott DA, et al.; APM: SE Working Group of the Australian and New Zealand College of Anaesthetists and Faculty of Pain Medicine. Acute Pain Management: Scientific Evidence. 3rd ed. Melbourne: ANZCA & FPM, 2010.
(21) Kissin I. Preemptive Analgesia. Anesthesiology 2000; 93:1138–43.
(22) McCartney CJL, Sinha A, Katz J. A qualitative systematic review of the role of N-Methyl-D-aspartate receptor antagonists in preventive analgesia. Anesth Analg 2004; 98:1385–400.
(23) Hirota K, Lambert DG. Ketamine: new uses for an old drug? Br J Anaesth 2011; 107:123–6.
(24) De Kock M, Lavand’homme P, Waterloos H. “Balanced analgesia” in the perioperative period: is there a place for ketamine? Pain 2001; 92:373–80.
(25) Lavand’homme P, De Kock M, Waterloos H. Intraoperative epidural analgesia combined with ketamine provides effective preventive analgesia in patients undergoing major digestive surgery. Anesthesiology 2005; 103:813–20.
(26) Gilron I, Bailey JM, Tu D, et al. Morphine, Gabapentin, or Their Combination for Neuropathic Pain. N Engl J Med 2005; 352:1324–34.
(27) Rowbotham DJ. Gabapentin: a new drug for postoperative pain? Br J Anaesth 2006; 96:152–5.
(28) Dirks J, Fredensborg BB, Christensen D, et al. A Randomized Study of the Effects of Single-dose Gabapentin versus Placebo on Postoperative Pain and Morphine Consumption after Mastectomy. Anesthesiology 2002; 97:560–4.
(29) Pandey CK, Navkar DV, Giri PJ, et al. Evaluation of the Optimal Preemptive Dose of Gabapentin for Postoperative Pain Relief After Lumbar Discectomy. J Neurosurg Anesthesiol 2005; 17:65–8.
(30) Clarke H, Bonin RP, Orser B, et al. The prevention of chronic postsurgical pain using gabapentin and pregabalin: a combined systematic review and meta-analysis. Anesth Analg 2012; 115:428–4.
(31) Vigneault L, Turgeon AF, Côté D, et al. Perioperative intravenous lidocaine infusion for postoperative pain control: a meta-analysis of randomized controlled trials. Can J Anaesth 2011; 58:22–37.
(32) Strichartz GR. Novel ideas of local anaesthetic actions on various ion channels to ameliorate postoperative pain. Br J Anaesth 2008; 101:45–7.
(33) Leeuw M, Goossens MEJB, Linton SJ, et al. The fear-avoidance model of musculoskeletal pain: current state of scientific evidence. J Behav Med 2007; 30:77–94.
(34) Crombez G, Vlaeyen JW, Heuts PH, et al. Pain-related fear is more disabling than pain itself: evidence on the role of pain-related fear in chronic back pain disability. Pain 1999; 80:329–39.
(35) Morley S. Psychology of pain. Br J Anaesth 2008; 101:25–31.
(36) Tracey I. Imaging pain. Br J Anaesth 2008; 101:32–9.
(37) Guzmán J, Esmail R, Karjalainen K, et al. Multidisciplinary rehabilitation for chronic low back pain: systematic review. BMJ 2001; 322:1511–16.
(38) Katz J, Poleshuck EL, Andrus CH, et al. Risk factors for acute pain and its persistence following breast cancer surgery. Pain 2005; 119:16–25.
(39) Hinrichs-Rocker A, Schulz K, Jänvinen I, et al. Psychosocial predictors and correlates for chronic post-surgical pain (CPSP)—A systematic review. Eur J Pain 2009; 13:719–30.
(40) Munafò MR, Stevenson J. Anxiety and surgical recovery. Reinterpreting the literature. J Psychosom Res. 2001; 51:589–96.
(41) Carr DB, Goudas LC. Acute pain. Lancet 1999;353:2051–8.
(42) Egbert LD, Battit GE, Welch CE, et al. Reduction of postoperative pain by encouragement and instruction of patients—a study of doctor-patient rapport. N Engl J Med. 1964; 270:825–7.
(43) Suls J, Wan CK. Effects of sensory and procedural information on coping with stressful medical procedures and pain: a meta-analysis. J Consult Clin Psychol 1989; 57:372–9.
(44) Baars JE, Markus T, Kuipers EJ, et al. Patients’ preferences regarding shared decision-making in the treatment of inflammatory bowel disease: results from a patient-empowerment study. Digestion 2010; 81:113–19.
(45) Kehlet H, Dahl JB. Anaesthesia, surgery, and challenges in postoperative recovery. Lancet 2003; 362:1921–






