Etiquetas
#pandemia #COVID-19 #triaje #toma de decisiones #comorbilidades #cuidados paliativos #Dolor crónico #Neurocirugía #Síndrome de Fracaso de Cirugía Espinal Lumbar #anestesia espinal unilateral #dosis mínima #lateralización #cirugía traumatológica ambulatoria #nervio pudendo #neuralgia #radiofrecuencia pulsada; ultrasonido. #dolor #dolor neuropatico #topiramato #dolor agudo postquirúrgico #dolor incisiona #anestesia #niños #dolor agudo #dolor quirurgico #modelos y teorias #enfermeria #noticias #Investigación en Servicios de Salud #Rehabilitación #ansiedad #emociones #miedo #tristeza #Parche #Buprenorfina #Fentanilo #problemas sociales #síndrome pediátrico inflamatorio multisistémico #fibromialgia #narrativas #experiencia #Afrontamiento #estados emocionales #dolor de espalda #Cuidado paliativo #opioidesRevista El Dolor 69 | Julio 2018 - Año 28 | Revisiones Bibliográficas
Redefiniendo Dolor Agudo Postoperatorio: Dolor Incisional
Recibido: 11-01-2018Aceptado: 03-03-2018
Páginas 26-30
Cabrera, María Carolina (1)
(1) Anestesiólogo. Profesor Auxiliar de Anestesiología Universidad de Valparaíso. Hospital Clínico FACH. Santiago. Chile.
El adecuado manejo perioperatorio del dolor agudo y la elección de la técnica anestésica influyen en la incidencia de complicaciones a corto, mediano y largo plazo, encontrándose en este grupo el desarrollo de dolor crónico no oncológico (DCNO). Debido al aumento de la prevalencia de dolor crónico no oncológico y su relación con un manejo inadecuado o insuficiente del dolor agudo en el periodo perioperatorio, hemos realizado una revisión de su fisiopatología, los factores de riesgo y las técnicas preventivas que permitirían mitigar y/o disminuir su incidencia.
Palabras Clave: dolor, dolor agudo postquirúrgico, dolor incisional.
The adequate perioperative management of acute pain and the correct choice of the anesthetic technique influence the incidence of complications in the short, medium and long term, being in this group the development of chronic non-oncological pain (CNOP). Due to the increase in the prevalence of non-oncological chronic pain and its relation with an inadequate or insufficient management of acute pain in the perioperative period, we have carried out a review of its pathophysiology, risk factors and preventive techniques that would allow mitigating and/or
decrease its incidence.
Keywords: pain, acute postoperative pain, incisional pain.
La práctica anestesiológica moderna se caracteriza por una búsqueda continua de alta seguridad y baja incidencia de eventos adversos en el perioperatorio de cada paciente. El dolor es uno de los más importantes eventos adversos postoperatorios, ya que se ha demostrado su relación con aumento de morbimortalidad, prolongación de estadía hospitalaria y baja satisfacción del paciente con su sistema de salud.
Así, en el sostenido y progresivo avance de la anestesiología, es que los médicos deben preocuparse y responsabilizarse de conocer la fisiopatología y manejar el dolor agudo postoperatorio.
En estos últimos años, se ha avanzado en forma importante en la investigación y en la comprensión de los mecanismos del dolor agudo y, específicamente, en el dolor agudo postoperatorio. Es importante reconocer al dolor agudo postoperatorio como una entidad única y diferente a los modelos de estudio de dolor agudo que tradicionalmente se estudian como el dolor agudo de inflamación producida por antígenos, inyección de formalina e inyección de capsaicina. El modelo tradicional de dolor agudo en que, luego de una noxa, hay una respuesta no se ajusta en el caso de una cirugía, ya que en el caso de esta se producen múltiples noxas de diferente intensidad y repetidas en el tiempo, hasta que el cirujano realice su última sutura. Por esto es que se ha creado un modelo particular para el dolor durante una cirugía que se ha definido como dolor incisional.
Dolor Incisional: Se ha demostrado que durante una cirugía, la nocicepción y el dolor son fenómenos dinámicos y no preestablecidos, donde su respuesta será diferente cada vez. El principal objetivo de todo el estudio fisiopatológico es lograr optimizar y modular los tratamientos, buscar nuevas áreas de desarrollo de terapias y así lograr el bienestar de los pacientes, teniendo un postoperatorio con el menor dolor posible.
La principal idea de trabajar con un modelo diferente es que contribuirá a entender el efecto y los mecanismos de las diferentes terapias y es la base fundamental de la analgesia preventiva y de la terapia multimodal analgésica postoperatoria. También permite comprender por qué no son extrapolables los resultados obtenidos en investigación en otros tipos de dolor agudo diferentes al dolor incisional.
Sin embargo, hoy en día, existe importante evidencia que demuestra que aún hoy muchos pacientes experimentan dolor en su postoperatorio. Apfelbaum publicó en 2003 una interesante revisión donde demostró que sobre el 40% de los pacientes experimentaban dolor luego de sus cirugías y hasta en un 15% de ellos este dolor era severo. Lo más interesante de este trabajo fue que comparó sus datos con los de 10 años previos y no logró demostrar diferencias a pesar del transcurso del tiempo, las nuevas terapias y la creación de unidades de dolor agudo. Esto pudiera explicarse por diferentes motivos, uno de los principales es por falta de conciencia respecto a la presencia de dolor luego de cualquier tipo de cirugía y a la falta de consensos por parte de los diferentes especialistas en cuanto a la necesidad de indicar y mantener las terapias analgésicas en el postoperatorio.
Una de las consecuencias más temidas de este dolor mal manejado es su cronificación que, en algunos tipos de cirugía, como, mastectomías, toracotomías puede llegar a valores superiores al 50% (Tabla 1).
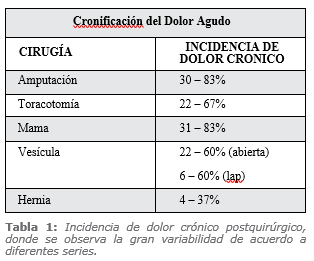
Fisiopatología: A continuación, se presenta una revisión de la fisiopatología del dolor agudo postoperatorio enfatizada en las áreas más novedosas y en desarrollo.
Neuroplasticidad
Sensibilización periférica y central: Una vez que el cirujano realiza la incisión quirúrgica, se produce una liberación importante de sustancias a nivel periférico por la disrupción de los tejidos y daño nervioso.
Estas sustancias, que se conocen como sopa inflamatoria, contienen entre otros prostaglandinas, bradiquininas, histamina y protones, que producen dolor e inflamación. Aunque la inflamación participa en la generación de dolor incisional, su rol sería diferente al compararlo con otros modelos de dolor agudo. Se ha determinado que en el dolor agudo postoperatorio la isquemia tisular y la acidosis local cumplen un rol fundamental. La acidosis activaría canales capaces de transducir dolor como receptores tirosinkinasa, purinérgicos y canales de potasio.
Una vez liberadas estas sustancias e inducida la transducción de diferentes canales, se genera una respuesta periférica aumentada frente a un mismo estímulo, fenómeno que se conoce como sensibilización periférica (Figura 1).
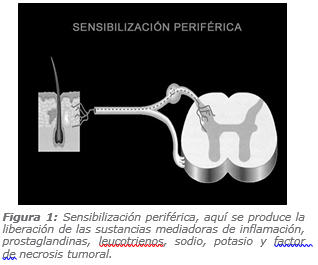
Esto significa que los canales de Na+ y Ca++ disminuyen su umbral de transmisión, favoreciendo la conducción de la respuesta dolorosa. Este fenómeno de sensibilización implica una alta frecuencia de respuesta a estímulos, aumento de la actividad espontánea y un aumento del área de respuesta. Clínicamente, esto se traduce en una respuesta nociceptiva aumentada frente a un mismo estímulo, generando hiperalgesia y alodinia.
La conducción de estos estímulos de dolor es por fibras A, delta y C. Las primeras mielinizadas y de transmisión rápida; y las segundas no mielinizadas de transmisión más lenta.
Se ha demostrado en estos últimos años que en la injuria tisular periférica además existe daño de nervios, por lo que el dolor neuropático también estaría involucrado en la génesis del dolor postoperatorio.
Las distintas fibras nerviosas van generando potenciales de acción que van siendo trasmitidos desde la periferia hacia la médula espinal.
A nivel del ganglio dorsal, se encuentra la primera neurona que envía una fibra eferente hacia la periferia y otra aferente que va hacia la médula espinal. Aquí se producen interesantes fenómenos que amplifican aún más esta respuesta dolorosa. Se ha detectado una importante producción de glutamato que irá a actuar al asta posterior de la médula espinal. También y en forma simultánea, se ha detectado la liberación de cantidades importantes de sustancia P, que también actuaría en el asta posterior de la médula espinal. Estas señales llegan a las láminas I, II, V de Rexed.
Sin duda, el lugar que más se ha investigado y que cumpliría un rol fundamental en el desencadenamiento, mantención y amplificación del dolor agudo postoperatorio es el asta posterior de la médula espinal. Aquí es donde se producen, en forma simultánea, una serie de mecanismos conocidos como sensibilización central, (Figura 2), que corresponden a una respuesta dolorosa amplificada a nivel del sistema nervioso central.
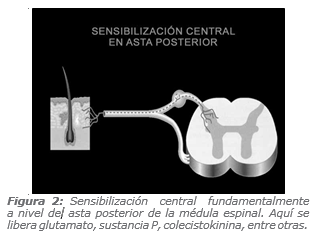
El desarrollo y mantención de la sensibilización central es objeto de amplio estudio. Es mediada por aferentes periféricos, pero una vez que se desarrolla se independiza de la actividad periférica de la herida. La sensibilización de las vías centrales del dolor implica dos hechos fundamentales:
1. Facilitación de respuestas sinápticas excitatorias.
2. Disminución o ausencia de actividad de vías inhibitorias. Se produce así amplificación de la respuesta, tanto a estímulos dolorosos, como estímulos indoloros.
El manejo del dolor incisional, como una entidad clínica especial, ha sido importante ya que se ha demostrado que la sensibilización a nivel del asta dorsal (central) cumple un rol fundamental el este tipo de dolor. Esto se debe a que el estímulo, en el caso de una cirugía, se mantiene mientras se generen nuevas injurias y así nuevos estímulos mantienen esta nueva respuesta facilitada y amplificada. También algunos grupos de investigadores consideran al dolor agudo postoperatorio como un tipo transitorio de dolor neuropático, donde la neuroplasticidad de la médula espinal jugaría un rol central y fundamental. Esto explica la efectividad demostrada en las investigaciones iniciales realizadas con fármacos que, tradicionalmente, se utilizaban solo en el manejo de dolor neuropático, como la gabapentina y pregabalina. Ambos fármacos reducirían el requerimiento y tolerancia a opioides, modulando la respuesta de sensibilización a nivel del sistema nervioso central.
A nivel del asta posterior en las láminas II, IV de Rexed se encuentran receptores N-Metil de aspartato (NMDA), G- Metil de aspartato (GMPA). En condición de reposo, éstos se encuentran bloqueados por Mg. Una vez que se une el glutamato, se produce una entrada importante de Calcio que genera depolarización de la segunda neurona a nivel de la médula espinal. Por este mecanismo es que la ketamina, potente inhibidor de NMDA, impide la liberación de mediadores al espacio intersináptico.
Existen tipos especializados de neuronas, como las de amplio rango (WDR), capaces de conducir impulsos nerviosos de las más variadas amplitudes, fenómeno conocido como windup.
Además, las neuronas del asta posterior van cambiando su forma de respuesta, de acuerdo a los estímulos que van recibiendo, fenómeno conocido como neuroplasticidad neuronal. Estos cambios en su rol transmisor normal son los que explicarían fenómenos como la hiperalgesia y la cronificación del dolor postoperatorio. En la actualidad, se considera que la persistencia anormal de la sensibilización central del sistema nervioso central es la causa más frecuente de dolor crónico. Así, todos estos estímulos que llegan de manera amplificada y facilitada al sistema nervioso central actúan en los receptores MOR (morfínicos), ampliamente distribuidos a nivel de neocórtex, tálamo, hipotálamo y médula espinal (Figura 3).
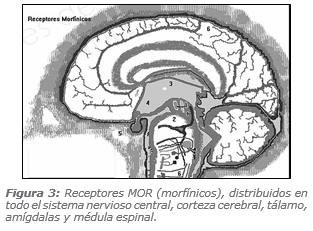
Se ha investigado y se ha generado gran controversia en cuanto al rol que cumplirían las vías descendentes inhibitorias del dolor. Aparentemente, las vías descendentes noradrenérgicas que modularían la transmisión y sensibilización espinal cumplen un rol bastante importante y la incorporación de fármacos que potencien esta respuesta, como el tapentadol serían de alta utilidad.
Hiperalgesia: Se define como la respuesta exagerada a un estímulo. La presencia de hiperalgesia tiene un impacto mayor en el procesamiento del dolor a nivel cortical y es expresión de la sensibilización del sistema nervioso central. Ésta genera un aumento del dolor que experimenta el paciente. Más dolor implica mayor sufrimiento del paciente y una mayor respuesta de stress. También se ha asociado al fenómeno de hiperalgesia y de sensibilización central, dependiendo de su magnitud, como una de las bases para la cronificación del dolor.
Su diagnóstico no es sencillo y sus causas son fundamentalmente dos:
1. Hiperalgesia inducida por nociceptores.
2. Hiperalgesia inducida por fármacos.
En el contexto de dolor agudo postoperatorio ambas pueden estar presentes y comparten mecanismos de acción como la activación de receptores NMDA.
La hiperalgesia inducida por nociceptores es una consecuencia del daño de los tejidos y de los nervios que desencadena los cambios antes mencionados y conocidos como neuroplasticidad. Inicialmente, estas transformaciones son de tipo excitatorio, esto es conocido como la activación (sensibilización), que es completamente reversible. Luego se generan cambios en la modulación, que aún son reversibles, pero que implican cambios en la función de la membrana celular. Para finalmente generarse cambios irreversibles con modificación del fenotipo, que implica muerte de algunas células e inducción de genes. Se considera la modificación como la base del dolor crónico, patológico. Estos procesos van ocurriendo en forma simultánea a nivel de la periferia, en la médula espinal y también a nivel de la corteza cerebral.
Por otra parte, es muy interesante y polémico el desarrollo de hiperalgesia inducida por fármacos, específicamente opioides, paradojalmente el analgésico más utilizado en el preoperatorio. Esta respuesta de hiperalgesia se debería a la activación simultánea de sistemas inhibitorios y facilitadores del dolor. La sensibilización aguda por opioides se debe al uso de altas dosis intraoperatorias y/o por cambios agudos en la concentración plasmática de estos. Cuál es la real importancia y magnitud de la hiperalgesia por opioides en el contexto del dolor agudo postoperatorio, se encuentra en etapa de investigación. Su expresión clínica es el aumento del dolor postoperatorio y un aumento de los requerimientos de morfina. También podría sumarse a la hiperalgesia nociceptiva y así reforzar la memoria dolorosa aumentando las probabilidades de dolor crónico postoperatorio.
Respuesta y procesamiento cortical: Una vez ocurridos todos estos cambios a nivel del asta dorsal, los estímulos son conducidos por los haces espinotalámicos hacia la corteza cerebral, tálamo y regiones menos conocidas como hipotálamo y língula. Estas regiones en forma integrada generarán una respuesta compleja y personal al estímulo doloroso.
Esta respuesta involucrará una reacción emotiva que será la calificación personal que hace el paciente de su dolor, una respuesta motora y una respuesta de estrés generalizado por la activación del sistema nervioso simpático.
Respuesta de estrés al dolor: Una de las grandes motivaciones del manejo del dolor agudo postoperatorio es evitar el sufrimiento de los pacientes y lograr así un postoperatorio más confortable.
Pero, sin duda alguna, una de las principales razones debe ser intentar abolir o disminuir la gran descarga simpática que se produce y que es responsable de la gran cantidad de consecuencias deletéreas que produce esta respuesta de stress para el paciente (Figura 4).

Activación sistema nervioso central: A este nivel, se produce una importante liberación de ACTH que activa al sistema adrenérgico, evidenciándose una respuesta generalizada del sistema simpático que involucra a todos los sistemas.
Respuesta cardiovascular: El aumento de epinefrina circulante activa los receptores α y β, produciéndose vasoconstricción y taquicardia. Esto hace que aumente el consumo de oxígeno miocárdico que, en pacientes portadores de cardiopatía coronaria, puede desencadenar fenómenos de isquemia miocárdica.
Respuesta adrenal: La médula suprarrenal libera una cantidad significativa de catecolaminas que aumentan y mantienen este estado de hiperdinamia generalizada.
Respuesta hepática: Como consecuencia de la activación simpática se produce aumento de la glicógenolisis, fenómeno que desencadena tendencia a la hiperglicemia postoperatoria.
Respuesta gastrointestinal: El sistema simpático es responsable de una disminución del peristaltismo gastrointestinal. Esta respuesta sistémica de estrés puede ser en parte responsable del íleo postoperatorio.
En conclusión, el conocimiento de la fisiopatología del dolor agudo postoperatorio (dolor incisional) permitirá entender las bases de los tratamientos y comprender las ventajas de bloquear la transmisión de la respuesta dolorosa a través de diferentes mecanismos, concepto básico conocido como analgesia multimodal.
Pero, también permitirá que el anestesiólogo lidere así al equipo de salud, demostrando que un adecuado alivio del dolor postoperatorio aumentará la satisfacción y confort del paciente con una clara disminución de morbimortalidad postoperatoria. Esto permitirá una recuperación postoperatoria más rápida y prevendrá la cronificación del dolor.
Finalmente, en la actualidad una analgesia balanceada basada en la combinación de fármacos analgésicos y antihiperalgésicos, debería asegurar un alivio del dolor agudo postoperatorio en forma segura y eficiente.






